
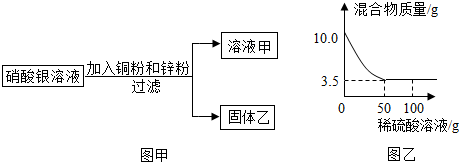
分析 ①根据金属活动性顺序及其运用分析.排在氢之前的金属可与稀盐酸或稀硫酸反应产生氢气,排在前面的金属(除钾、钙、钠外)可将排在后面的金属从其盐溶液中置换出来结合实验的现象进行分析.
②根据题意,锌与稀硫酸反应生成硫酸锌和氢气;由反应的实验情况图,完全反应后剩余固体的质量为3.5g,即铜锌合金样品中含铜的质量为3.5g;则锌的质量为10g-3.5g=6.5g;由参加反应的锌的质量,计算出参加反应硫酸的质量,进而可计算出所用稀硫酸溶液中溶质的质量分数.
解答 解:①实验后,溶液甲呈蓝色,说明含有铜盐,则锌粉不足,因此向固体乙上滴加盐酸时没有气泡产生;由金属活动性顺序及其运用可知,金属活动性Al>Zn>Cu>Ag,所以锌粉优先与AgNO3发生反应,铜粉后与AgNO3发生反应,由于锌粉量的不足,没有把硝酸铜溶液中的铜置换出来,因此溶液甲一定含有反应生成的Zn (NO3)2和剩余的Cu(NO3)2,可能含有AgNO3,滤渣中一定含有被置换出的银,可能含有铜,由以上分析可知,
Ⅰ.由于锌不足,因此向固体乙上滴加盐酸时没有气泡产生;固体乙中金属的成分是银或银和铜;
Ⅱ.溶液甲中一定含有的溶质是Cu(NO3)2、Zn(NO3)2;使溶液呈蓝色的化学反应是Cu+2AgNO3=Cu(NO3)2+2Ag (写化学方程式),该反应的基本类型是置换反应;
②Ⅰ.由反应的实验情况图,完全反应后剩余固体的质量为3.5g,即铜锌合金样品中含铜的质量为3.5g,则锌的质量为10g-3.5g=6.5g,故混合物中Zn的物质的量是$\frac{6.5g}{65g/mol}$=0.1mol.
Ⅱ.设反应中消耗稀硫酸溶液中溶质的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 98
6.5g x
则$\frac{65}{98}=\frac{6.5g}{x}$,解得x=9.8g.
所用稀硫酸溶液中溶质的质量分数为:$\frac{9.8g}{50g}$×100%=19.6%.
答:所用稀硫酸溶液中溶质的质量分数是19.6%.
故答案为:
①Ⅰ. 银或银和铜.
Ⅱ. Cu(NO3)2、Zn(NO3)2. Cu+2AgNO3=Cu(NO3)2+2Ag,置换反应.
②Ⅰ. 0.1.Ⅱ.19.6%
点评 本题考查了金属活动性顺序的运用,主要考查了对金属活动性顺序的应用和理解,培养学生的应用能力和解决问题的能力;掌握根据化学方程式的计算即可正确解答本题.


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:初中化学 来源: 题型:解答题
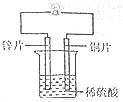 为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验.
为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验.| 锌 | 铜 | 镍 | 铜 | |
| 稀硫酸的质量分数 | 5% | 5% | 15% | 15% |
| 反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 甲 | 乙 | 丙 | 丁 |  |
| 分子示意图 | 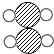 |  |  |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 凡是均一、稳定的液体一定是溶液 | |
| B. | 只有固体才可以作为溶质 | |
| C. | 硝酸铵、氢氧化钠溶于水,均会放出热量 | |
| D. | 将少量碘放入汽油中,搅拌,可以得到碘的汽油溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭在氧气中燃烧,发出白光 | |
| B. | 打开盛有浓盐酸的瓶盖,瓶口出现白雾 | |
| C. | 铜片投入到稀硫酸中,产生大量的气泡 | |
| D. | 将冷碟子放在蜡烛火焰的上方,碟底出现黑色物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 白色粉末中肯定没有硫酸铜,可能有氢氧化钠和氯化钠 | |
| B. | 白色粉末中肯定有氯化钡、氢氧化钠、硫酸钠和碳酸钠 | |
| C. | 白色粉末中肯定有氯化钡、硫酸钠和碳酸钠,可能有氢氧化钠和氯化钠 | |
| D. | 若在滤液中滴加稀盐酸产生气泡,则白色粉末中肯定有碳酸钠和氯化钡,且二者的质量比可能为$\frac{{m(N{a_2}C{O_3})}}{{m(BaC{l_2})}}$>$\frac{106}{208}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com