
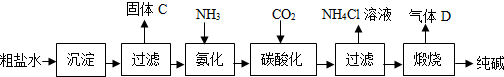
分析 (1)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
(2)氯化钠、水、二氧化碳、氨气等物质反应生成碳酸氢钠和氯化铵;
(3)NH4Cl中含有氮元素,可用作氮肥.
(4)该工艺流程中,可以循环使用物质是二氧化碳.
(5)碳酸钠受热不易分解,而碳酸氢钠受热分解生成碳酸钠、水和二氧化碳.
解答 解:(1)粗盐水加入沉淀剂NaOH、Na2CO3分别除去MgCl2、CaCl2,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠固体C为氢氧化镁、碳酸钙;
反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl,Na2CO3+CaCl2═CaCO3↓+2NaCl.
故填:氢氧化镁、碳酸钙;MgCl2+2NaOH=Mg(OH)2↓+2NaCl,或 Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,该反应化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
故填:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
(3)“碳酸化”后过滤获得NH4Cl中含有氮元素,可用作氮肥.
故填:氮.
(4)该工艺流程中,可以循环使用物质是二氧化碳.
故填:二氧化碳.
(5)鉴别纯碱产品中是否含有碳酸氢钠方法是:把样品适量置于试管中加热,把导管通入澄清石灰水中,如果澄清石灰水变浑浊,说明样品中含有碳酸氢钠,反之则没有.
故填:把样品适量置于试管中加热,把导管通入澄清石灰水中,如果澄清石灰水变浑浊,说明样品中含有碳酸氢钠,反之则没有.
点评 本题主要考查物质的性质,只有掌握了物质的性质,才能够对各种问题作出正确的解答.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中,向其中加入碳酸钠溶液 | 有气泡产生 | 猜想二正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 92克 | B. | 90.2克 | C. | 9.8克 | D. | 29.3克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com