
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由质量守恒定律,混合物减少的质量即为生成二氧化碳气体的质量,由反应的化学方程式列式计算出参加反应的碳酸钙的质量、稀盐酸中溶质的质量、生成氯化钙的质量,进而进行分析解答即可.
解答 解:由质量守恒定律,反应生成二氧化碳的质量为12g+50g-57.6g=4.4g.
设参加反应的碳酸钙的质量为x,稀盐酸中溶质的质量为y,生成氯化钙的质量为z
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
x y z 4.4g
(1)$\frac{100}{44}=\frac{x}{4.4g}$ x=10g
该石灰石中碳酸钙的质量分数为$\frac{10g}{12g}$×100%≈83.3%;
(2)$\frac{73}{44}=\frac{y}{4.4g}$ y=7.3g
稀盐酸中溶质的质量分数为$\frac{7.3g}{50g}×$100%=14.6%;
(3)$\frac{111}{44}=\frac{z}{4.4g}$ z=11.1g
反应后所得溶液中溶质的质量分数为$\frac{11.1g}{10g+50g-4.4g}$×100%≈20.0%.
答:(1)该石灰石中碳酸钙的质量分数为83.3%;
(2)稀盐酸中溶质的质量分数为14.6%;
(3)反应后所得溶液中溶质的质量分数为20.0%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 蒸馏水 | B. | 煮沸不久的硬水 | ||
| C. | 纯净水 | D. | 长期放置的矿泉水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO2 | O2 | 通过灼热的铜网 |
| B | KOH溶液 | K2CO3 | 加入足量稀盐酸至不再产生气泡 |
| C | CuCl2 | CaCO3 | 溶解、过滤、蒸发 |
| D | H2 | H2O | 通过浓H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
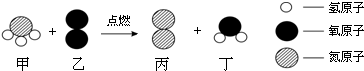
| A. | 该反应属于化合反应 | B. | 一定条件下,丁可转化为乙 | ||
| C. | 反应中甲、乙的分子数比为1:1 | D. | 反应前后元素的化合价都改变了 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
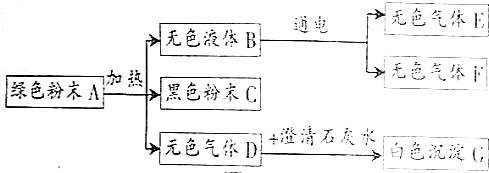
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 家里电器着火,立刻用水扑灭 | |
| B. | 楼层高的室内着火,立刻打开门窗 | |
| C. | 室内着火,火势较大,应该卧着向外爬出 | |
| D. | 家里油锅着火,立刻用水浇灭 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com