
某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明做了如下实验:准确称取样品12.0g,向其中加入57.9g稀盐酸,恰好完全反应,共产生气体4.4g,请回答下列问题:
(1)小明要从反应后的溶液中提取NaCl应采用的方法是 ;
(2)纯碱样品中的Na2CO3的质量分数是多少?(结果保留一位小数,要求写出计算过程)
(3)反应后所得溶液中NaCl的质量分数是多少?(要求写出计算过程)
(1)蒸发结晶 (2)(3)
解析试题分析:(1)由于氯化钠的溶解度随温度的升高而变化不大,故要从反应后的溶液中提取NaCl应采用的方法是:蒸发结晶
(2)根据反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑,可知产生气体4.4g,即为二氧化碳的质量,再根据CO2与Na2CO3的质量关系,即可求出Na2CO3的质量,进而计算出纯碱样品中的Na2CO3的质量分数,同时根据CO2与NaCl的质量关系,即可求出反应后溶液中NaCl的质量,进而可计算反应后所得溶液中NaCl的质量分数
解:设Na2CO3的质量为x,NaCl的质量为y
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
106:44=x:4.4g
x=10.6g
故纯碱样品中的Na2CO3的质量分数=10.6g/12g×100%=88.3%
(3)117:44=y:4.4g y=11.7g
故反应后溶液中的NaCl的质量=11.7g+(12.0g-10.6g)=13.1g
反应后所得溶液中NaCl的质量分数=13.1g/(12.0g+57.9g-4.4g)×100%=20%
考点:结晶的方法,根据化学方程式计算,溶质质量分数的计算


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:单选题
工业上以CaO和HNO3为原料制备Ca(NO3)2?6H2O晶体.为确保制备过程中既不补充水,也无多余的水,所用硝酸的溶质质量分数约为( )
| A.41.2% | B.53.8% | C.58.3% | D.70.0% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素。
(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是 (填序号)。
①KCl; ②NH4HCO3; ③Ca3(PO4)2。
(2)“测土配方”可以实现“缺什么、补什么”,使用该技术的好处是 。
(3)某同学取丰收牌钾肥(如图1)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图2。试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(反应方程式为:K2SO4+BaCl2=BaSO4↓+2KCl,杂质不参加反应。)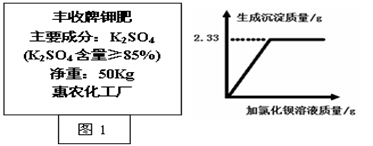
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(5分)铜镁合金常用作飞机天线等导电材料。欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金10g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 8.5 | 7 | 6.6 | 6.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= .
(2)通过计算,上述过程中同时产生H2的质量为 g.
(3)计算电解后剩余溶液中NaC1的质量分数(写出详细的计算过程,结果精确到0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(10分)实验室有瓶标签模糊的烧碱溶液,小军测量其溶质质量分数的操作如下:
①取一洁净的锥形瓶称量,其质量为25.5g,往其中注入一定量上述烧碱溶液,并滴入1滴酚酞溶液后,又称量锥形瓶,质量为37.5g;
②取质量分数为24.5%的稀硫酸逐滴滴入上述锥形瓶中,边滴边振荡,当观察到溶液由红色变为无色时,停止滴液。再次称量锥形瓶,质量为51.0g
请解答下列问题:
(1)所取烧碱溶液的质量 = g。(注:滴人酚酞的质量忽略不计)
(2)反应所消耗的稀硫酸质量= g。
(3)通过计算确定该瓶烧碱溶液的溶质质量分数。(列出计算过程)
(4)问题讨论:小亮做同样的实验得到的结果与小军的结果有差异。于是小亮测自己实验后锥形瓶内溶液的pH,pH =6.2,则小亮的结果比小军的 (选填“偏大”或“偏小”或“无影响”),原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
我国制碱工业的先驱——侯德榜探索发明了“侯氏制碱法”,其生产过程涉及的主要化学反应如下:
①NH2+CO2+X=NH4HCO3
②NH4HCO3+NaCl=NH4Cl+NaHCO3↓
③2NaHCO3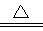 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
请回答下列问题:
(1)反应①中X的化学式为 。
(2)除去混在Na2CO3粉末中少量的NaHCO3的方法是 。
(3)工业纯碱中含有氯化钠,取55g工业纯碱,向其中加入269.5g稀盐酸,恰好完全反应,生成22g二氧化碳,求:
①工业纯碱中碳酸钠的质量分数。(计算结果保留到0.1%)
②反应后溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分)为综合利用生产过程中的副产品CaSO4,某化工厂设计了以下制备(NH4)2SO4的工艺流程: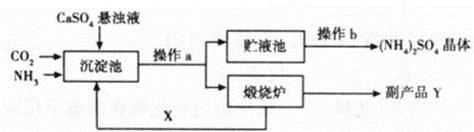
(1)此流程中,在沉淀池发生的化学反应为CO2+2NH3+CaSO4+H2O==CaCO3↓+ (NH4)2SO4
在煅烧炉中发生的化学反应方程式为 ;该工艺中可循环使用的X为 (填化学式);副产品Y有何用途 (填一种即可)。
(2)从贮液池中获得(NH4)2SO4晶体要进行操作b,操作b是 。若经过一定处理后的贮液池中,形成30℃时(NH4)2SO4的饱和溶液,则此时溶质质量分数为 (已知30℃时硫酸铵的溶解度为78g)。
(3)欲制备6.6t (NH4)2SO4晶体,理论上需要CaSO4多少吨?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com