
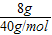 =0.2mol;
=0.2mol;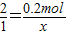


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:
某废水200g,其中含硫酸0.15mol,加入一定量的氢氧化钠溶液,可使废水酸性降低。
①在上述废水中加入80g10%的氢氧化钠溶 液,可以中和多少mol的硫酸?
液,可以中和多少mol的硫酸?
(1)
②上述反应结束后,恢复到室温,所得溶液的pH (2) (填“﹥”、“=”或“﹤”)7。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com