
【题目】2018年12月8日,嫦娥四号探测器在西昌卫星发射中心由长征三号乙运载火箭成功发射。2019年1月3日,嫦娥四号探测器成功着陆月球背面。
(1)发射嫦娥四号运载火箭的燃料有偏二甲肼(C2H8N2),发射时与助燃剂四氧化氮(N2O4)剧烈反应,![]() ,X的化学式为_______。
,X的化学式为_______。
(2)嫦娥四号降落相机镜筒由钛合金制作。甲图是钛的原子结构示意图,乙图摘自元素周期表,部分信息略去则Y=______。
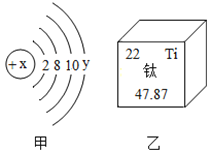
(3)月球表面富含钛铁矿,其主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为______。
【答案】N2 2 +4
【解析】
(1)由反应的化学方程式C2H8N2+2N2O4![]() 3X+2CO2+4H2O,反应前后C、H、N、O原子的个数分别为
3X+2CO2+4H2O,反应前后C、H、N、O原子的个数分别为
反应前 反应后
C原子 2 2
H原子 8 8
N原子 6 0
O原子 8 8
根据化学变化前后原子的种类、数目不变,生成物X的3个分子中含有6个N原子,则每个X分子由2个N原子构成,物质X的化学式为N2;
(2)原子中,核电荷数=核内质子数=核外电子数;y=22-2-8-10=2;
(3)铁元素显+2价,氧元素显-2价,设钛元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×3=0,则x=+4价。
故填:(1)N2;
(2)2;
(3)+4。


科目:初中化学 来源: 题型:
【题目】如图是实验室用于气体制备的装置,请根据图示回答问题:
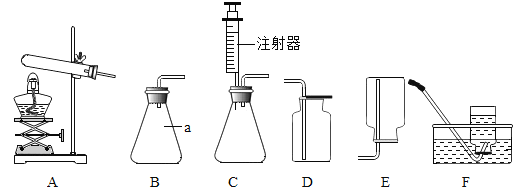
(1)图中a装置的名称是______。
(2)实验室中能用于过氧化氢溶液制氧气,且便于随时添加液体药品的发生装置是______(填序号,下同);要想得到比较纯净的氧气,需要选择的收集装置是______。
(3)实验室制取二氧化碳时,应选择的收集装置是______,理由是______;判断二氧化碳是否收集满的方法是______,制备二氧化碳气体的方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某种铁的冶炼流程如下图所示。下列说法错误的是
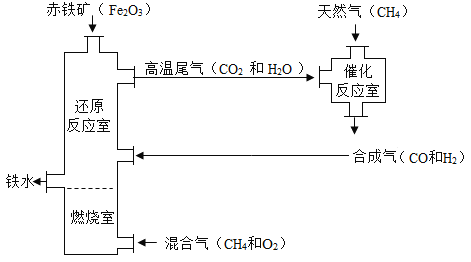
A.“燃烧室”中CH4燃烧的作用是提供一氧化碳
B.整个流程中,有四种元素化合价发生改变
C.流程中CH4可循环使用
D.催化室中发生的总反应化学方程式可能为:2CH4 +H2O +CO2  3CO+ 5H2
3CO+ 5H2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属及其化合物的应用及制备。
(一)铁、铜的广泛应用
(1)航母用钢要具有低磁性。下列具有磁性的是______(填序号)。
A FeO B Fe3O4 C Fe2O3
(2)“航母”螺旋浆可由特制的铜合金制造。铜合金比铜的硬度______(填“大”或“小”)。铜比铁在海水中耐腐蚀的原因是______。
(3)生铁炼钢时,硅(Si)与氧化亚铁在高温条件下转化为二氧化硅和铁,该反应的化学方程式为______。
(二)硫酸铜的制备
下图为某兴趣小组用含较多杂质的铜粉制取硫酸铜晶体[CuSO4·5H2O]的两种实验方案。
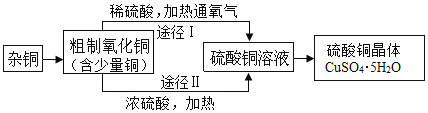
(4)制备中需过滤得到硫酸铜晶体。过滤时需要的玻璃仪器有烧杯、玻璃棒和___。
(5)灼烧杂铜除去其中的杂质,产生CO2和少量CO。灼烧后的产物为CuO及少量Cu。产物中含有Cu的可能原因是______(填序号)。
A灼烧过程中,部分氧化铜与一氧化碳反应
B灼烧不充分,铜未被完全氧化
C该条件下铜无法被氧气氧化
(6)方案Ⅰ通入氧气,少量Cu转化为CuSO4。该反应的化学方程式为____。
(7)方案Ⅱ中加入浓硫酸发生的反应有Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
方案Ⅰ优于方案Ⅱ的理由是____。
(三)波尔多液的制备及组成测定
波尔多液是常见的杀菌剂,为天蓝色碱性悬浊液。以硫酸铜、生石灰及水为原料,制备波尔多液。为测定从波尔多液中分离出的天蓝色固体[CuSO4·aCu(OH)2·bCa(OH)2·cH2O]的组成,设计如下实验:
(实验Ⅰ)称取64.4g天蓝色固体,加入足量稀HNO3使其完全溶解,再加入过量Ba(NO3)2溶液,过滤,洗涤干燥得白色固体23.3g。
(8)判断Ba(NO3)2溶液已过量的方法是:静置,向上层清液中滴加____溶液,无现象。
(9)不能在铁制容器中配波尔多液。请用化学方程式解释原因____。
(实验Ⅱ)另取64.4g天蓝色固体,用下图装置进行热分解实验:
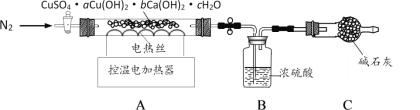
(资料)①CuSO4、Cu(OH)2、Ca(OH)2在一定温度下能受热分解,分别生成两种氧化物,分解过程中各元素的化合价均不改变。
②天蓝色固体在110℃时,完全失去结晶水。
③Cu(OH)2在100℃时分解完全。CuSO4和Ca(OH)2在580℃左右时开始分解,到650℃时均能分解完全。
④浓硫酸可用于吸收SO3。
(10)按图连接好装置,实验前要先__________。
(11)控制温度在110℃充分加热,测得B装置增重10.8g。再升温至650℃充分加热,B装置又增重了15.2 g。最终剩余固体中的成分是_________。
(12)整个加热过程中,天蓝色固体分解生成水的总质量为_________g。
(13)天蓝色固体CuSO4·aCu(OH)2·bCa(OH)2·cH2O中,a∶b∶c=______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌钙片的有效成分为碳酸钙,还含有淀粉等物质。化学小组取M克的钙片利用如下装置,测定其中钙元素的质量分数。(装置气密性良好;每片中其他物质不含何元素且不参与反应;稀盐酸的挥发忽略不计)
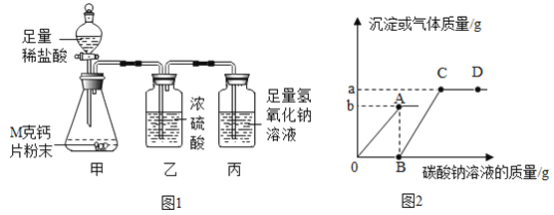
(1)能否通过称量反应前、后丙集气瓶及其中溶液的质量,达成实验目的,说明理由。
____________________。
(2)反应结束后,过滤锥形瓶中浊液。向所得滤液中逐滴加入碳酸钠溶液,所加碳酸钠溶液的质量与产生沉淀或气体的质量关系如图象所示。回答下列问题:
Ⅰ.写出滴加碳酸钠溶液的过程中观察到的现象_____________________。
Ⅱ.B点至C点的反应过程中,溶液的pH(填“逐渐变大”、“逐渐变小”或“不变”)_______;CD段(不含C点)所示溶液中的溶质是_______。
Ⅲ.结合图象,确定钙片中钙元素质量分数的表达式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组在实验室发现一瓶氢氧化钠溶液,瓶口有少量白色固体且玻璃瓶塞打不开,这一情况激起了他们浓厚的兴趣,于是展开了如下探究:
(提出问题)
瓶口白色固体的成分是什么?
(查找资料)
(1)玻璃中含有二氧化硅(SiO2),试剂瓶身经抛光处理,不易反应,而瓶口和玻璃塞上的磨砂将二氧化硅裸露出来。
(2)二氧化硅能与氢氧化钠溶液反应,![]()
(3)硅酸钠(Na2SiO3)是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性;硅酸钠溶液能与强酸反应,如:![]() (白色);硅酸钠溶液能与氯化钙溶液反应:
(白色);硅酸钠溶液能与氯化钙溶液反应:![]() (白色)。
(白色)。
(作出猜想)
白色固体的成分是:1.硅酸钠:Ⅱ,硅酸钠和碳酸钠:Ⅲ硅酸钠、碳酸钠和氢氧化钠
(实验探究)
取一定量白色固体溶于适量水中形成样品溶液,分组进行如下实验并相互评价:
实验操作 | 实验现象 | 结论与评价 | ||
第 一 组 |
| 有气泡冒出且产生白色沉淀 | 同学们认为猜想____不成立 | |
第 二 组 | 第 一 步 |
| 产生白色沉淀 | 第一组的同学认为:此步骤还不能准确判断出原固体的成分。原因是________ |
第 二 步 |
| _______ | 大家一致认为: 猜想Ⅱ成立 | |
(解释结论)
猜想Ⅱ中碳酸钠的来源是________(用化学方程式表示)。
(反思交流)
(1)有同学认为,第二组实验中不能用氢氧化钙溶液代替氯化钙溶液,理由_______;
(2)氢氧化钠溶液必须密封保存,且试剂瓶只能用橡胶塞或软木塞。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氨碱法生成纯碱的主要反应原理知下:(1)![]() ;(2)
;(2)![]() ,对上述信息的有关理解不正确的是()
,对上述信息的有关理解不正确的是()
A.(1)中析出碳酸氢钠晶体后剩余溶液只有一种溶质
B.二氧化碳的作用是提供碳、氧元素
C.氨盐水比食盐水更易吸收二氧化碳,是因为氨盐水呈碱性
D.反应(1)中生成碳酸氧钠而不是碳酸钠,是因为碳酸氢钠更易达到饱和而结晶析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F是初中化学的常见物质,A与B的组成元素相同,D、E在通常状况下是气体,C可用来改良酸性土壤,F是大理石的主要成分。其转化关系如下图所示,部分反应物、生成物和反应条件未标出。
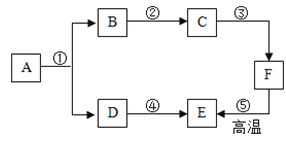
(1)A的化学式为_________;
(2)反应②的主要现象是_________。
(3)反应③的化学方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com