CaC
2+2H
2O═Ca(OH)
2+C
2H
2↑ B C b 2C
2H
2+5O
2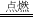
2H
2O+4CO
2 KClO
3和MnO
2 氧气不易溶于水 2KClO
3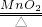
2KCl+2O
2↑ 用水湿润 过氧化氢和二氧化锰 2H
2O
2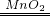
2H
2O+O
2↑ B E
分析:①根据方程式的书写方法考虑;
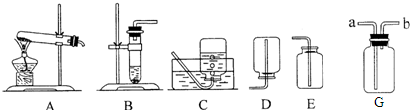
②根据发生装置主要取决于反应物的状态和反应条件,收集装置主要取决于气体的密度、溶水性分析;
③根据方程式的书写方法考虑;
④根据装置图来反推反应物的状态,根据收集装置反推气体的性质,再利用方程式的书写方法来写出方程式;
⑤根据玻璃管和橡皮管的连接方法考虑,根据装置图来反推反应物的状态,进而选出反应物写出方程式;
⑥根据发生装置主要取决于反应物的状态和反应条件,收集装置主要取决于气体的密度、溶水性分析.
解答:①由题给信息可知电石与水反应的反应物是电石、水,生成物是氢氧化钙和乙炔(C
2H
2),用观察法配平即可;
②反应装置的选择分为:固固加热型、固液不加热型,电石是固体,水是液体,所以不需要加热,发生装置选择B,用排水法收集到的气体比较纯,用排空气法收集到的气体比排水法收集到的气体干燥;由于乙炔的密度比空气小,所以从短管进入;
③乙炔燃烧的反应物是乙炔和氧气,生成物是二氧化碳和水,反应条件是点燃,用奇偶法配平即可;
④由于A装置中需要加热,所以反应物可以是氯酸钾,二氧化锰作催化剂,由于氧气不易溶于水,所以可以用排水法收集气体;反应物是氯酸钾,生成物是氯化钾和氧气,用最小公倍数法配平;
⑤连接玻璃管和橡皮管时,先将玻璃管在水中湿润,再旋转着插入橡皮管中;由B装置不需要加热,用过氧化氢和二氧化锰制取氧气即可,反应物是过氧化氢,生成物是水和氧气,二氧化锰作催化剂,用奇偶法配平即可;
⑥实验室用大理石和稀盐酸反应制取二氧化碳气体,属于固液在常温下反应制取气体,应选择发生装置是B;二氧化碳的密度比空气大,能溶于水,用向上排空气法收集;
故答案为:①CaC
2+2H
2O═Ca(OH)
2+C
2H
2↑;②B;C; b;③2C
2H
2+5O
2
2H
2O+4CO
2;④KClO
3和MnO
2;氧气不易溶于水; 2KClO
3
2KCl+2O
2↑;⑤用水湿润;过氧化氢和二氧化锰;2H
2O
2
2H
2O+O
2↑;⑥B;E.
点评:利用改进后的装置收集气体时(排空气法收集气体)如果收集密度比空气“大”的气体,要从“长”的一端进,收集密度比空气“小”的气体,要从“短”的一端进,排水法收集气体时要从“短”的一端进.


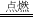 2H2O+4CO2 KClO3和MnO2 氧气不易溶于水 2KClO3
2H2O+4CO2 KClO3和MnO2 氧气不易溶于水 2KClO3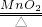 2KCl+2O2↑ 用水湿润 过氧化氢和二氧化锰 2H2O2
2KCl+2O2↑ 用水湿润 过氧化氢和二氧化锰 2H2O2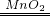 2H2O+O2↑ B E
2H2O+O2↑ B E 2H2O+4CO2;④KClO3和MnO2;氧气不易溶于水; 2KClO3
2H2O+4CO2;④KClO3和MnO2;氧气不易溶于水; 2KClO3 2KCl+2O2↑;⑤用水湿润;过氧化氢和二氧化锰;2H2O2
2KCl+2O2↑;⑤用水湿润;过氧化氢和二氧化锰;2H2O2 2H2O+O2↑;⑥B;E.
2H2O+O2↑;⑥B;E.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案