
【题目】小华同学做“人体吸入空气和呼出的气体成分差异探究”实验时,分别收集两瓶空气样品和两瓶人体呼出的气体,进行探究。如图,关于这两个实验的说法中正确的是
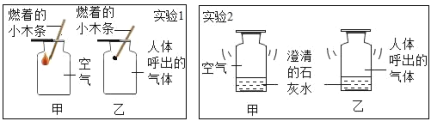
A. 实验1中,甲、乙两瓶里木条燃烧的现象不同
B. 实验1和2都能证明人体呼出的气体中氧气含量减小了
C. 实验1和2中发生的反应均属于分解反应
D. 实验2中,甲瓶的澄清石灰水无明显变化表明空气中无二氧化碳
科目:初中化学 来源: 题型:
【题目】氯化钙(CaCl2)可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含有少量Al2O3、Fe2O3、SiO2等杂质)制备氯化钙的主要流程如下:

请回答下列问题:
(1)配制31%的稀盐酸730 g,需要36.5%的浓盐酸______g。
(2)酸溶时碳酸钙参与反应的化学方程式为_______。
(3)滤渣I的成分为____,滤渣II中含有Al(OH)3和______。
(4)过滤使用到的玻璃仪器有____。操作I采用的方法是:蒸发浓缩、_____、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学用如图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管,点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5,下列对这两种现象解释不合理的是( )

A. 甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
B. 甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
C. 乙同学可能没夹紧弹簧夹,红磷燃烧时外界空气进入瓶中
D. 乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一无色液体A,在通电条件下,可以产生B和H两种单质气体。其它关系如图所示,请完成下列问题。
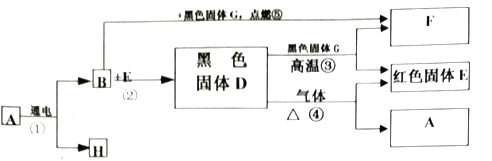
(1)写出反应②的基本反应类型_____。
(2)写出有关物质的化学式:A是_____,G是_____。
(3)写出反应①的化学方程式_____。
(4)写出反应③的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学用天平称取3.6克氯酸钾(1克以下用游码)过程中把砝码和药品的位置放颠倒了,则该同学称得的氯酸钾的实际质量为()
A. 3.6克B. 2.4克C. 4.2克D. 无法确定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,市场上销售的一种真空充气包装的形如小枕头的“蛋黄派”, 它“鼓鼓”的包装和松软的口感受到人们的关注。请用所学知识探究以下问题:

(1)“鼓鼓”的袋内所充气体的作用是________。
(2)小明同学认为袋内无色无味的气体是氮气,并用燃着的木条检验他的猜想.请你评价该检验方法的可行性:_________________(简述理由)。
(3)小红同学猜想是二氧化碳。请你帮助她设计一个简单的实验方案,用以验证其猜想是否正确:
实验步骤 | 现象和结论 |
________________ | ________________________ |
(4)你认为食品充气包装,对所充气体的要求是:
①____________; ②_________; ③_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气中氧气含量测定的再认识。


[经典赏析]教材中介绍了科学家_____用定量的方法研究了空气的成分(实验装置如图1)。
[实验回顾]实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),
写出红磷燃烧的文字表达式:_____。
兴趣小组用该方法测出的氧气含量常常远低于1/5。
[进行猜想]
(1)装置漏气;
(2)_____装置内氧气有剩余;
(3)_____。
[实验与交流]在老师的指导下,小明对实验后瓶中的气体进行了观察,并用燃着的木条伸入瓶中,他看到的现象是_____,由此可以推测瓶中剩余气体的物理性质_____、化学性质_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对氯酸钾(KClO3)展开如下探究:
(探究一)工业制备KClO3
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
(资料卡片):氯化时,主要反应为6Ca(OH)2 + 6X ═ Ca(ClO3)2 + 5CaCl2 + 6H2O,少量 X与Ca(OH)2反应生成Ca(ClO)2、CaCl2和H2O,Ca(ClO)2 分解为CaCl2和O2。
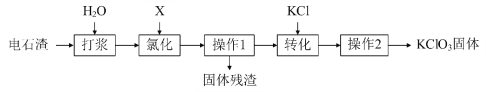
(1)根据资料,X的化学式为______,写出氯化时,X和Ca(OH)2反应生成Ca(ClO)2的化学方程式______。
(2)氯化时,为提高X转化为Ca(ClO3)2的转化率,下列措施可行的是______(填序号)。
A.充分搅拌浆料 B.加足量水使Ca(OH)2完全溶解 C.缓缓通入X
(3)操作1在实验室中的名称是______,需要用到的玻璃仪器有______、______和玻璃棒,玻璃棒的作用是______。氯化过程控制电石渣过量,固体残渣的主要成分为______和______(填化学式)。
(4)操作1后得到溶液中Ca(ClO3)2与CaCl2的化学计量数之比______1:5(填“>”、“<”或“=”)。转化时,加入KCl发生反应的化学方程式为______。
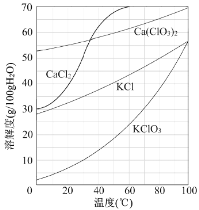
(5)操作2包含一系列实验操作,结合如图分析,主要操作为蒸发浓缩 →______→过滤→洗涤→低温烘干。
(探究二)探究KClO3制氧气
某小组利用如图所示装置对KClO3制氧气进行了探究:
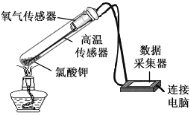
(资料卡片):
①KClO3的熔点约为356℃,MnO2在加热条件下不分解。
②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率示意图如下:
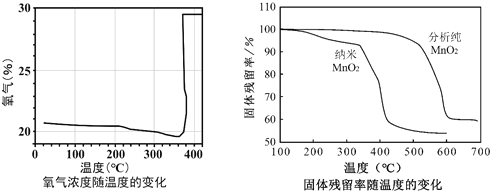
(6)由图可知KClO3分解温度______(填“高于”、“等于”或“低于”)其熔点。
(7)图中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是______。
(8)分析图中,对KClO3分解催化效果更好的催化剂是______。
(9)将3.06gKClO3和MnO2混合物以4:1配比加热至完全反应,可得氧气体积约为多少升____?(写出计算过程,计算时精确到小数点后两位。已知氧气密度约为1.43g / L。)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于溶液的说法错误的是( )
A. 溶液是由溶质和溶剂组成的混合物
B. 向100g溶质质量分数为30%的硝酸钾溶液中加入20mL水,溶液的溶质质量分数变为25%
C. 试剂瓶中的溶液在使用时不慎洒出一部分,剩余溶液的溶质质量分数减小
D. 溶液加水稀释前后,溶质的质量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com