
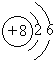 是氧原子的结构示意图,那么,1mol 氧气分子中含有9.632×1024个电子.
是氧原子的结构示意图,那么,1mol 氧气分子中含有9.632×1024个电子.分析 可以根据概念的含义进行分析、考虑,从而得出正确的结论.要充分理解每摩尔物质含有6.02×1023个该物质的微粒的含义.
解答 解:(1)物质的量与物质的质量、物质的数量是不同的物理量.故填:不同.
(2)1个硝酸分子中含有1个氢原子、3个氮原子,根据物质的量的含义可知,1mol硝酸中含有 6.02×1023个H原子,含有1.806×1024个O原子.
(3)1个氧分子中含有16个电子,根据物质的量的含义可知,1mol氧气分子中含有6.02×1023个氧分子,1mol氧气分子中含有16×6.02×1023(或9.632×1024)个电子.氧原子核外有2个电子层,位于第二周期.
故填:(1)不同;(2)6.02×1023,1.806×1024;
(3)9.632×1024,2.
点评 本题主要考查了一种新的物理量“物质的量”相关方面的知识.可以依据已有的知识进行.


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
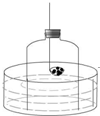 如图所示装置(燃烧匙中盛放的是红磷)可用于实验室测定空气中氧气的含量,将燃烧匙中红磷点燃后迅速伸入玻璃钟罩内,塞紧橡皮塞.根据实验现象回答下列问题:
如图所示装置(燃烧匙中盛放的是红磷)可用于实验室测定空气中氧气的含量,将燃烧匙中红磷点燃后迅速伸入玻璃钟罩内,塞紧橡皮塞.根据实验现象回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验 | 实验现象 | 实验分析、结论 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ①产生大量气泡 | ②反应速率适中,气体便于收集 |
| 实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 2 | 49.21 | |
| ④ | 30 | 5 | 55 | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线(图1).
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线(图1).| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com