
| A. | HClO3 | B. | KHSO4 | C. | H2S | D. | H2SO4 |
科目:初中化学 来源: 题型:选择题
| A. | 溶液的pH值不变 | B. | 溶液的质量不变 | ||
| C. | 溶液中溶质的质量分数减小 | D. | 溶液中溶质的溶解度先增大后不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镉元素 | B. | 金属镉 | C. | 一个镉原子 | D. | 一个镉分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁和氧气等于氧化镁 | |
| B. | 镁和氧气在点燃的条件下,生成氧化镁 | |
| C. | 48份质量的镁欲2份质量的氧气发生化学反应生成80份质量的氧化镁 | |
| D. | 每两个镁分子与一个氧气分子在点燃的条件下生成两个氧化镁分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 所选的物质 | 所看见的现象或者反应方程式 | |
| 方案一 | 水 | 易溶于水的是氢氧化钠,不能完全溶解的是氢氧化钙 |
| 方案二 | 碳酸钠溶液 | 产生沉淀的是氢氧化钙,无现象的是氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
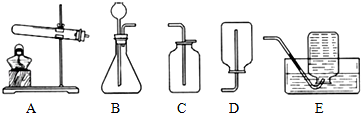 实验室常用如图所示的装置制取气体和气体性质的验证,回答有关问题.
实验室常用如图所示的装置制取气体和气体性质的验证,回答有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
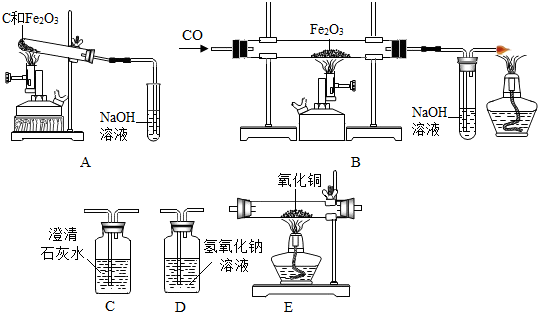
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com