
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
| A. | 表中m的值为2.8 | |
| B. | X中氧元素的质量为1.6g | |
| C. | 增加氧气的量可以减少X的生成 | |
| D. | 物质X一定含有1.2g碳元素,可能含有氢元素 |
分析 根据质量守恒定律可知:反应后质量减少的物质是反应物,质量增加的物质是生成物.
通过计算乙醇、氧气、二氧化碳、水中各元素的质量,根据质量守恒定律可以确定X的组成、质量和化学式;
经计算知X是一氧化碳,说明乙醇没有充分燃烧,增加氧气的量有助于乙醇的充分燃烧,从而减少一氧化碳的生成.
解答 解:由于乙醇和氧气反应后质量减少,二氧化碳和水反应后质量增加,
根据质量守恒定律可知:在该反应中,乙醇和氧气是反应物,二氧化碳和水是生成物.
由化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数可以计算出:
4.6g乙醇中碳、氢、氧三元素的质量分别是2.4g、0.6g、1.6g;
4.4g二氧化碳中碳、氧两元素的质量分别是1.2g、3.2g;
5.4g水中氢、氧两元素的质量分别为0.6g、4.8g.
因此反应物中共有2.4g碳元素、0.6g氢元素、9.6g氧元素,
生成物二氧化碳和水中共有1.2g碳元素、0.6g氢元素、8g氧元素.
根据质量守恒定律可知:反应物中有1.2g碳元素和1.6g氧元素进入了生成物X中,
说明生成物X由碳、氧两元素组成,X中不含氢元素,其质量为1.2g+1.6g=2.8g,所以m的值为2.8.
由于X在反应前的质量为0,反应后的质量为2.8g,
说明X在反应过程中质量有变化,不符合催化剂的特点,所以X不是该反应的催化剂.
设X的化学式为CxOy,则12x:16y=1.2g:1.6g,解得x:y=1:1,即X的化学式为CO.
由于反应生成了一氧化碳,说明乙醇燃烧不充分,增加氧气的量,有助于乙醇的充分燃烧,从而减少一氧化碳的生成.
故选D.
点评 本题主要考查化合物中某元素的质量的计算,难度较大.本题的关键有:
一、反应物和生成物的确定
二、X的元素组成、质量和化学式的确定
三、氧气在该反应中的作用.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:初中化学 来源: 题型:解答题
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
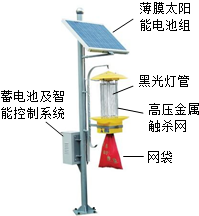 如图是一个太阳能黑光灯灭虫装置,上方的薄膜太阳能电池组将太阳能转化成电能,为诱虫的黑光灯及高压金属触杀网供电.
如图是一个太阳能黑光灯灭虫装置,上方的薄膜太阳能电池组将太阳能转化成电能,为诱虫的黑光灯及高压金属触杀网供电.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg+O2═MgO2 | B. | H2O2═H2↑+O2↑ | ||
| C. | 2Fe+3H2SO4═Fe2(SO4)3+3H2↑ | D. | CO2+Ca(OH)2═CaCO3↓+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验次序 | H2O2溶液的质量分数 | H2O2溶液 用量/毫升 | 物质D 用量/克 | 反应温度/℃ | 收集气体 体积/毫升 | 所需时间/秒 |
| ① | 0.30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 0.15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 0.15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 0.5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 0.30 | 5 | 0 | 55 | 2 | 10.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是甲、乙两种物质的溶解度曲线,请回答下列问题:
如图是甲、乙两种物质的溶解度曲线,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com