
| A. | 化学变化中分子种类发生改变,分子种类发生改变的变化一定是化学变化 | |
| B. | 氧化物中含有氧元素,含氧元素的化合物一定是氧化物 | |
| C. | 碱的溶液能使无色酚酞试液变红,能使无色酚酞试液变红的一定是碱的溶液 | |
| D. | 酸碱中和反应有水生成,有水生成的反应一定是酸碱中和反应 |
分析 A、根据化学变化的实质,进行分析判断.
B、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
C、根据显碱性的不一定是碱溶液,也可能是盐溶液,进行分析判断.
D、中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水.
解答 解:A、化学变化的实质是分子分成原子,原子再重新组合成新分子,化学变化中分子种类发生改变,分子种类发生改变的变化一定是化学变化,故选项推理正确.
B、氧化物中含有氧元素,但含氧元素的化合物一定是氧化物,如Na2CO3,故选项推理错误.
C、碱的溶液能使无色酚酞试液变红,能使无色酚酞试液变红的不一定是碱的溶液,也可能是盐溶液,故选项推理错误.
D、酸碱中和反应有水生成,有水生成的反应不一定是酸碱中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项推理错误.
故选:A.
点评 本题难度不大,掌握碱的化学性质、中和反应的特征、氧化物的特征、化学变化的实质等是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | P+O2$\frac{\underline{\;点燃\;}}{\;}$P2O3 | ||
| C. | 2H2$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
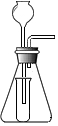 如图所示是某同学设计的一套制取二氧化碳的简易装置,装置中小试管的作用是A.
如图所示是某同学设计的一套制取二氧化碳的简易装置,装置中小试管的作用是A.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
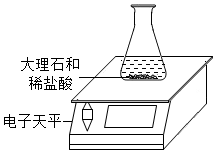 某同学对“影响稀盐酸和大理石反应快慢的因素”进行探究.选取的药品:成分相同的粉末状大理石、块状大理石两种样品;浓度为16%、9%的稀盐酸.采用控制变量法设计实验方案,以5分钟内收集到CO2的质量作为判断依据.已知稀盐酸足量且样品中杂质不与稀盐酸反应,实验装置如图.读取电子天平的示数,据此计算生成的CO2的质量,记录的数据如表
某同学对“影响稀盐酸和大理石反应快慢的因素”进行探究.选取的药品:成分相同的粉末状大理石、块状大理石两种样品;浓度为16%、9%的稀盐酸.采用控制变量法设计实验方案,以5分钟内收集到CO2的质量作为判断依据.已知稀盐酸足量且样品中杂质不与稀盐酸反应,实验装置如图.读取电子天平的示数,据此计算生成的CO2的质量,记录的数据如表| 实验序号 | 大理石 (各6g) | 稀盐酸的浓度 | 反应开始到5分钟产生CO2的质量 | 反应结束产生的CO2的质量 |
| ① | 块状 | 16% | 2.16g | 2.2g |
| ② | 块状 | 9% | 1.42g | 2.2g |
| ③ | 粉末 | 16% | 2.33g | 2.2g |
| ④ | 粉末 | 9% | 1.93g | m2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
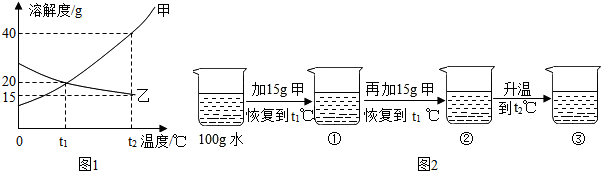
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
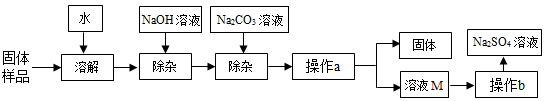
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com