
【题目】某兴趣小组的同学们整理了一些无明显现象的化学反应,如①二氧化碳与水反应;②二氧化碳与氢氧化钠反应;③盐酸与氢氧化钠反应。
提示:碳酸钠溶液显碱性。
(实验探究)为了证明这些化学反应的发生同学们设计了如下方案:
组别 | I | II | Ⅲ |
实验操作 |
|
|
|
实验现象 | _______ | 无色酚酞溶液变红 | 溶液由红色变为无色 |
实验结论 | 证明CO2可与H2O反应 | 证明CO2可与NaOH反应 | 证明盐酸可与NaOH反应 |
(得出结论)同学们—致认为,只有III组的方案设计是合理的,写出其反应的化学方程式______________。在①②③的三个反应中,属于复分解反应的是________________(填序号)。
(评价反思)(1)I组设计的方案不严谨,请你说明理由__________________。
(2)同学们对II组的设计方案进行改进,都能充分证明CO2可与NaOH发生了化学反应。
改进实验方案 | 实验现象 |
[方案1]取二氧化碳通入氢氧化钠溶液后的液体少许于试管中,滴加足量的_______________ | _________- |
[方案2]分别向两个收集满CO2气体的等体积的软塑料瓶中加入约1/3体积的水和NaOH溶液,立即旋紧瓶,振荡 | __________(填“左”或“右”) 瓶变瘪的程度更大。 |
(归纳总结)同学们总结得出:证明无明显现象的化学反应发生的方法有:①_____________;②______________。
【答案】紫色石蕊试液变红 NaOH +HCl == NaCl + H2O ③ 盐酸挥发的氯化氢溶于水,使紫色石蕊试液变红 稀盐酸 产生气泡 右 证明反应物的减少 证明生成物的生成
【解析】
[实验探究]酸性溶液能使紫色石蕊试液变红,将二氧化碳通入紫色石蕊试液,试液变红,说明二氧化碳和水反应生成了碳酸;
[得出结论] 碱性溶液能使酚酞试液变红,第III组的方案设计是合理的,滴加盐酸过程中酚酞试液由红色变成无色,说明盐酸和氢氧化钠能反应,反应方程式为:NaOH +HCl == NaCl + H2O,是由两种物质相互交换成分生成两种新的化合物的复分解反应;
[评价反思] (1)I组设计的方案不严谨,理由是二氧化碳常用石灰石和和稀盐酸反应制取,盐酸有挥发性,可能是挥发的氯化氢溶于水,使紫色石蕊试液变红;
(2)[方案1]取二氧化碳通入氢氧化钠溶液后的液体少许于试管中,滴加足量的盐酸,有气泡产生,说明二氧化碳和氢氧化钠反应了,因为二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和盐酸反应生成二氧化碳,产生气泡,而氢氧化钠和盐酸反应无明显现象;
[方案2]分别向两个收集满CO2气体的等体积的软塑料瓶中加入约1/3体积的水和NaOH溶液,立即旋紧瓶,振荡,右边倒入氢氧化钠溶液的瓶变瘪的程度更大。
[归纳总结]由上述实验总结得出:证明无明显现象的化学反应发生的方法有:①证明反应物的减少;②证明生成物的生成。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题。
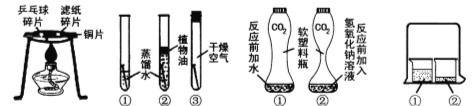
A. 燃烧的条件 B. 铁钉生锈的条件 C. 证明CO2与NaOH反应 D. 分子运动的现象
(1)通过实验A,可以说明燃烧的条件之一是 ,实验中使用铜片,是利用了铜的 性(填一条物理性质)
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水和 直接接触。欲除去铁锈可用 洗的方法,铁制品除锈时 (填“能”或“不能”)长时间浸在酸溶液中。
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2 与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 。
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的。当烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为 色;当烧杯①中液体换成浓盐酸,且烧杯②中液体换成滴有酚酞的NaOH溶液时,一段时间后,溶液颜色的变化是 。其中盐酸与NaOH反应的化学方程式为 ,属于
反应(填反应类型)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,B能用于灭火,“﹣”表示相连两物质之间能相互反应.
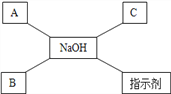
(1)按物质分类,C属于_____(填“氧化物”、“酸”、“碱”或“盐”)。
(2)写出C的一种物质与NaOH反应的化学方程式:______。
(3)NaOH与A反应的实验现象是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
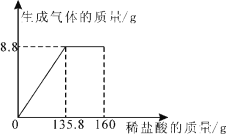
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:参加反应稀盐酸的溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
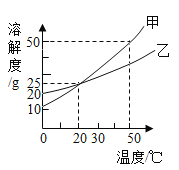
A.20℃时,100g甲溶液中含甲物质的质量小于25g
B.20℃时,等质量甲、乙饱和溶液中含溶质的质量相等
C.30℃时,甲物质的溶解度大于乙物质的溶解度
D.50℃时,将甲、乙两种物质的饱和溶液分别降温至20℃,析出晶体的质量甲大于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】质量守恒定律的发现对化学的发展做出了巨大贡献。
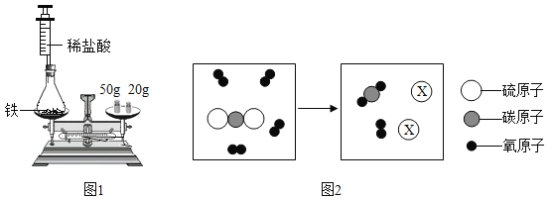
(1)为验证质量守恒定律,小华设计如图1所示装置进行实验。实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡(如图1所示),然后取下装置,用针筒向锥形瓶中注入少量稀盐酸,反应结束后再将装置放置于天平上,观察到_____,从而验证了质量守恒定律。若只将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是_____。
(2)某反应的微观示意图如图2所示。
①X的化学式是_____。
②根据上述微观示意图,可得出反应前后改变的是_____(填具体微粒名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】资源利用与社会可持续发展密切相关。
(1)水是一种生活中不可缺少的物质。
①下列能溶于水形成溶液的是_______(填字母序号,下同),所得溶液pH>7的是______;
a 纯碱 b 蔗糖 c 面粉 d 食用油
②生活中可以采用____________方法降低水的硬度;
(2)煤的气化和液化是实现能源清洁化的重要途径。水煤气中H2和CO在加热、加压和催化剂条件下可以合成液体燃料甲醇(CH3OH),该反应中H2和CO的质量比为___________。水煤气(H2和CO)在不同催化剂的作用下,还可以合成其他物质。仅以其为原料不可能化合得到的物质是__________ (填字母序号);
a 草酸(H2C2O4) b 乙酸(C2H4O2) c 尿素[CO(NH2)2]
(3)金属钯是稀有的贵重金属之一。现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动性。
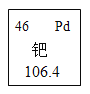
①在元素周期表中,钯元素的信息如图所示,对图中信息解释不正确的是__________;
a 原子序数为46 b 质子数为46 c 相对原子质量为46
②把钯戒指放入稀硫酸中,戒指完好无损,可推测钯在金属活动性顺序表中位于铁之________(填“前”或“后”);
③如图所示,将银、铂戒指分别放入甲、乙两试管溶液中,一段时间后取出,发现只有银戒指表面有明显变化。通过该实验判断,银、铂、钯的金属活动性由强到弱顺序为______________(用元素符号表示);

④将钯粉置于盐酸中,边通入氧气边搅拌,钯粉溶解得到二氯化钯(PdCl2)溶液,该反应的化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图:
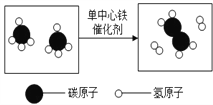
有关转化的说法正确的是( )
A. 催化剂反应前后质量不变,作用只能是加快反应
B. 该反应的化学方程式是:2CH4 = C2H4 + 2H2
C. 反应前后分子的种类发生了改变,是分解反应
D. 保持氢气化学性质的最小粒子是H
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生活和生产中有广泛的应用。某次实验结束后的废液中含有CuSO4、ZnSO4、FeSO4,几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
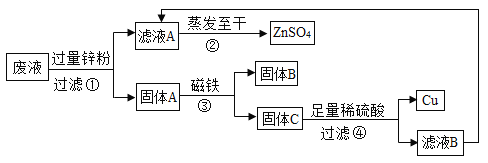
(1)通过上述实验,可以推断出在Cu、Zn、Fe三种金属中,金属活动性最强的是____。
(2)证明向固体C中加入的稀硫酸已经足量的方法是____。
(3)若实验过程中的物质损失可以忽略,要计算原废液中硫酸锌的质量分数,必须称量废液的质量、蒸发得到固体硫酸锌的质量和____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com