
【题目】酒精是一种常用的燃料,酒精的化学式为C2H6O。
(1)酒精由_____种元素组成,其中碳、氢元素的物质的量之比为_____。
(2)酒精的摩尔质量为_____,92g酒精的物质的量为_____mol,3mol酒精分子中碳原子的个数约为_____个。
(3)取75mL酒精与25mL蒸馏水充分混合后的体积_____(填小于、等于或大于)100mL,原因是_____。
(4)酒精在空气中燃烧生成二氧化碳和水,其反应的化学方程式为_____。
【答案】3 1:3 46g/mol 2 3.612×1024 小于 分子间有间隙 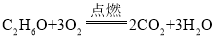
【解析】
(1)由酒精的化学式C2H6O可知,酒精由碳、氢、氧三种元素组成;物质的量=![]() ,所以,其中碳、氢元素的物质的量之比为2:6=1:3;
,所以,其中碳、氢元素的物质的量之比为2:6=1:3;
故填:3;1:3。
(2)摩尔质量在数值上等于相对分子质量,故酒精的摩尔质量为46g/mol;物质的量=![]() ,故92克酒精的物质的量=
,故92克酒精的物质的量=![]() =2mol;1mol任何物质中微粒的个数都大约是6.02×1023,故其中3mol酒精分子中碳原子的个数为3×2×6.02×1023=3.612×1024;
=2mol;1mol任何物质中微粒的个数都大约是6.02×1023,故其中3mol酒精分子中碳原子的个数为3×2×6.02×1023=3.612×1024;
故填:46g/mol;2;3.612×1024。
(3)取75mL酒精与25mL蒸馏水充分混合后的体积小于100mL,原因是分子间有间隙。
故填:小于;分子间有间隔。
(4)酒精在空气中燃烧生成二氧化碳和水,其反应的化学方程式为: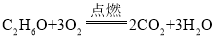 。故填:
。故填: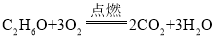 。
。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
【题目】用下列方法配制的溶液,其溶质质量分数为5%的是 ( )
A. 称取5.0g氯化钾,溶解在95mL水中,充分搅拌
B. 称取5.0g生石灰,放入95mL水中,充分搅拌
C. 量取5.0mL浓盐酸,倒入95mL水中,充分搅拌
D. 称取5.0g碳酸钙,放入95mL水中,充分搅拌
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据原子结构的知识和如图的信息填空
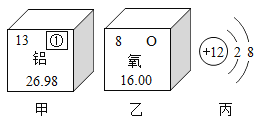
(1)甲图中①代表的元素符号是________,乙图中所示元素原子的核电荷数是________,丙图所示粒子属于________(填“原子”、“阳离子”或“阴离子”)。
(2)甲、乙、丙三种元素间最本质的区别是________(填字母)。
A质子数不同 B中子数不同 C相对原子质量不同
(3)写出甲、乙两种元素的单质间发生反应的化学方程式________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我校化学兴趣小组就空气中氧气的含量进行实验探究:
[集体讨论]:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(填编号)_____,
A 蜡烛 B 红磷 C 硫粉
为了充分消耗容器中的氧气,药品的用量应保证_____。
(2)测定空气中氧气体积分数的实验装置如图所示。在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧。
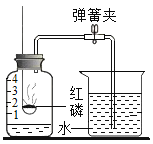
①写出红磷在空气中燃烧的文字表达式:_____
②待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此可知氧气约占空气总体积的_____。
③红磷熄灭后,集气瓶内剩下的气体主要是_____,该气体_____(填“支持”或“不支持”)燃烧。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号表示:
(1)两个钙原子______
(2)4个二氧化硫分子______
(3)水______
(4)2个亚铁离子______
(5)氧化镁中的镁元素呈正二价______
(6)两个碳酸根离子______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用甲和乙反应制备丙和丁,其反应的微观示意图如下:
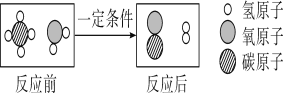
(1)该化学变化中没有发生改变的粒子是_______(填“分子”或“原子”)
(2)写该反应的化学方程式__________________。
(3)该反应中含氢元素的化合物有_____种;反应前后化合价发生了变化的元素是________(填元素符号)。
(4)反应物和生成物中属于氧化物的有____ 种,生成物中____ (填“有”或“没有”)单质。
(5)该化学反应的微观实质是_____________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示装置,向试管里的水中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质可能是
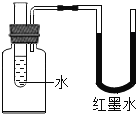
A.氯化钠B.氢氧化钠C.硝酸铵D.蔗糖
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在日常生活、工农业生产和科学研究中具有广泛的用途。小刚在实验室里配制100g10%的氯化钠溶液,操作如下图,请回答下列问题:
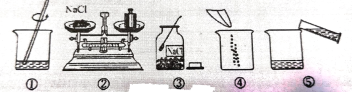
(1)该实验操作顺序为________(填序号 )。配制该溶液时需要NaCl固体_______g,需要水_____mL (水的密度为1g/mL),需要用________的量筒(填“50mL”、“100mL或“200mL" )量取。读数时,视线要与量筒内凹液面的最低处_______。
(2)配制该溶液的主要步骤有计算、称量、_______;操作①中玻璃棒的作用是________。
(3)经检验所得溶液的溶质质量分数偏低。请从实验操作上分析造成原因_________(写一点即可)。
(4)取上述溶液10g加水稀释到_______g,可得到5%的氯化钠溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com