
【题目】某化学兴趣小组的同学对空气中氧气的含量测定进行再探究。

(一)甲组同学利用某脱氧剂测定空气中氧气含量,兴趣小组进行了如下实验:
使用图1装置进行实验.实验前应先进行的操作是 。
【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末(体积为2mL),封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化。
【数据处理】
(1)实验中需要记录的数据是:① 。
②反应后注射器活塞进入后显示剩余气体的体积。
(2)上述实验测定过程至少需要重复两次,其目的是 。
【实验对比】
实验室常通过燃烧红磷法测定空气中氧气的含量(装置如图2)。步骤如下:
(1)用弹簧夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞。
(3) 。
(4)观察并记录水面的变化情况。
多次实验发现,集气瓶内上升的水面始终小于瓶内原有空气体积的。
【拓展研究】查阅资料得知,当空气中氧气的体积分数降至约为7%以下时,红磷不再燃烧.由此可知,燃烧红磷法测定结果不够准确。
【实验评价】与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是 。
(二)乙组同学利用装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%。
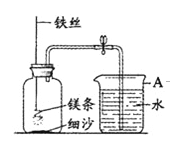
(1)如图中A仪器的名称是____________。
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有 。
【查阅资料】镁条在空气中燃烧,能与氧气反应产物为氧化镁(MgO)固体,也能与氮气反应产物为氮化镁(Mg3N2)固体。
(3)现有24g镁条,在空气中完全燃烧后,生成物的质量应在 (填数值范围)之间。
(请写出计算过程)
【答案】(一)检查装置的气密性 .
【数据处理】(1)注射器中原来的空气的体积(2)使测量的结果更准确(或者避免实验的偶然性)
【实验对比】(3)燃烧结束,冷却至室温。
【实验评价】不受氧气含量多少的影响,能充分消耗所有氧气,使结果更准确。
(二)(1)烧杯(2)21,氧气和氮气(3)33.3g--40g
【解析】
试题分析:(一)实验前应先进行的操作是检查装置的气密性;(1)注射器中原来的空气的体积(2)使测量的结果更准确(或者避免实验的偶然性)
【实验对比】(3)燃烧结束,冷却至室温。
【实验评价】不受氧气含量多少的影响,能充分消耗所有氧气,使结果更准确。
(二)(1)烧杯(2)氧气约占空气体积分数的21%,而氮气占78%,从而可判断只消耗氧气时,气体减少原体积的21%;而气体减少达70%时,大部分气体被消耗,说明减少的气体已不完全为氧气了,还应消耗了占空气78%的部分氮气;(3)设24g镁分别与氧气、氮气反应生成的氧化镁、氮化镁的质量分别为X、Y,2Mg~~2MgO 3Mg~~Mg3N2
48 80 72 100
24g X 24g Y
X=40g;Y=33.3g
由计算可知,24g镁在空气中完全燃烧后,生成物的质量大于33.3g,小于40g.33.3g--40g


科目:初中化学 来源: 题型:
【题目】在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量变化情况如图所示,下列说法正确的是( )
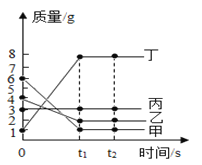
A.该物质为分解反应
B.丙一定是该反应的催化剂
C.该化学反应中甲、丁的质量变化之比为5:7
D.该化学反应中乙、丁的质量变化之比为1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】完成下列化学方程式并回答有关问题:
(1)二氧化碳通入澄清石灰水,观察到的现象是 。
(2)实验室用双氧水和二氧化锰混合制取氧气的文字表式 ,该反应属于 反应类型。
(3)电解水实验中,正极上收集到的是 气,正极与负极产生气体的体积比是 。
(4)点燃红磷的文字表达式 ,该反应属于 反应类型。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】填写出下列各仪器的名称,并回答下列问题

① ② ③

④ ⑤ ⑥
其中:⑤ (名称),用于 和 少量 。注意:用过后应立即 再去吸其他药品,防止污染。
⑥ (名称),用于量度 体积。注意:不能 ,不能 也不能 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活有密切联系。下列说法错误的是
A. pH<5.6的雨水称为酸雨
B. PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性
C. “温室效应”主要是由CO2等气体引起的
D. 生产中加速石油、煤炭的开采,可快速提高人类的生活质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室欲配制1000 g溶质质量分数为4%的氢氧化钠溶液。请回答下列问题;
(1)配制步骤
①计算:需氢氧化钠固体 g,水 mL(水的密度是1 g/cm3)。
②称量:用质量为23.1 g的烧杯作称量容器,托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在 盘。
③溶解:将氢氧化钠固体溶于水,用玻璃棒搅拌,使氢氧化钠全部溶解,冷却至室温。
④装瓶:把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。
在装有所配制溶液的试剂瓶(见图)标签上标明相应的两个信息为:__________________
(2)在配制过程中,导致溶液中氢氧化钠质量分数小于4%的可能原因是( )
①用量筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③在托盘天平的左盘称取氢氧化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数;④盛装溶液的试剂瓶用蒸馏水润洗;⑤氢氧化钠固体不纯。
A.①②③④⑤ B.只有①②④⑤ C.只有①②⑧ D.只有②③④⑤
(3)若老师提供的药品有500 g 8%的氢氧化钠溶液,500 g 1%的氢氧化钠溶液,足量的氢氧化钠固体和水,除了上述配制方案外,还可以用500g1%的氢氧化钠溶液,再加____________________来进行配制.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C、D四种粒子的结构示意图,E是硒元素在元素周期表中的信息,请回答下列问题:
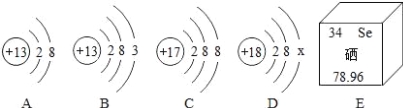
(1)图中A、B、C、D四种粒子中属于同种元素的是 ,属于阳离子的是 (填字母)。
(2)D中x= 。
(3)A、B、C、D四种粒子中具有稳定结构的原子是 (填字母)。
(4)E中硒元素的相对原子质量是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关注健康,预防疾病。下列叙述正确的是( )
A. 人体通过食物获得的蛋白质在胃肠道内与氧气发生反应,生成氨基酸
B. 维生素有20多种,在人体内都不能合成,只能从食物中摄取
C. 每克油脂在人体内完全氧化,放出的能量比糖类多,是重要的供能物质
D. 铁、锌、锡、碘、氟都是人体所需的微量元素。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com