
 2016年3月1日,合肥地铁1号线首列车正式上线调试,1号线预计2016年12月31日正式开通.
2016年3月1日,合肥地铁1号线首列车正式上线调试,1号线预计2016年12月31日正式开通.分析 金属材料包括金属单质和合金两大类;合金,是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,属于混合物.铁生锈的条件是和水、氧气同时接触解答;盐酸与氧化铁反应生成氯化铁和水.
解答 解:(1)1号线首列车中属于金属材料的是:铝合金外壳;
(2)地铁轨道所用材料锰钢属于混合物;锰钢能加工成铁轨说明金属具有延展性;
(3)铁生锈的条件是和氧气、水同时接触;
盐酸与氧化铁反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.
答案:
(1)铝合金外壳;
(2)混合物;延展;
(3)H2O;Fe2O3+6HCl=2FeCl3+3H2O.
点评 解答本题的关键是要充分理解物质的性质,只有理解了物质的性质才能确定物质的用途.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 细铁丝在空气中剧烈燃烧,火星四射,有黑色固体生成 | |
| B. | 红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾 | |
| C. | 少量高锰酸钾固体溶于水可得到浅绿色溶液 | |
| D. | 电解水时,正极和负极产生的气体体积比为1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 工业污水必须处理达标后再排放 | |
| B. | 使用淘米水浇花,浇菜可以节约用水 | |
| C. | 地球上储水量丰富,但可被利用的淡水资源较少 | |
| D. | 利用沉降的方法可将硬水转化成软水 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 反应的化学方程式 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
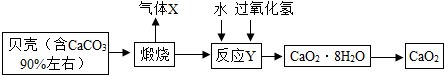
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com