
【题目】某同学对碳及碳的化合物知识进行了归纳、整理,并建构了如图所示的转化关系图。请回答下列问题。
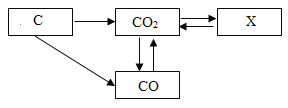
(1)物质X的化学式可以为H2CO3或_________:
(2)常温下,CO2通过化合反应转化成X的化学方程式为_________:
(3)C和CO都可以将金属从它们的氧化物中冶炼出来是因为它们都具有_____性;
(4)以下除去CO2中少量的CO方案中,能达到实验目的的是_______。
a将混合气体点燃
b将混合气体通过炽热的焦炭
c将混合气体通过炽热的氧化铜
【答案】CaCO3 CO2 +H2O=H2CO3 还原 c
【解析】
本题考查碳和碳的化合物之间的转化关系,应用化学方程式和化学式进行解答。
(1)从图框可知物质X和二氧化碳可以相互转化,实现相互转化方法有两种:1、二氧化碳与水反应生成碳酸,碳酸分解生成二氧化碳和水;2、二氧化碳与碱溶液反应生成碳酸盐和水,碳酸盐与酸反应可生成二氧化碳,例如二氧化碳与氢氧化钙溶液反应生成碳酸钙,碳酸钙与盐酸反应可生成二氧化碳气体。所以物质X的化学式可以为CaCO3。
(2)常温下,二氧化碳与水反应生成碳酸,碳酸分解生成二氧化碳和水,因此,CO2通过化合反应转化成X的化学方程式为CO2 +H2O=H2CO3:
(3)C和CO都可以将金属从它们的氧化物中冶炼出来是因为它们都具有还原性,在加热或高温条件下可以夺取金属氧化物中的氧,使金属氧化物发生还原反应,制得金属。
(4)以下除去CO2中少量的CO方案中,a将混合气体点燃,因为混合气体中没有氧气,不能点燃除去一氧化碳,不能达到实验目的; b将混合气体通过炽热的焦炭,二氧化碳会与炭反应生成一氧化碳,不能除去一氧化碳,反而除去了二氧化碳,不能达到实验目的;
c将混合气体通过炽热的氧化铜,一氧化碳具有还原性,能与氧化铜反应生成二氧化碳,能达到实验目的。故选c。


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:
【题目】在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净后在天平上称得质量为56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉一起放在天平上称量,记录所称得质量m1.将上述铁钉浸到硫酸铜溶液中,待反应一段时间后溶液颜色改变时,将盛有硫酸铜溶液和锥形瓶放在天平上称量,记录所称的质量为m2。
(1)m1_____m2(填“>”或“=”或“<”)。
(2)锥形瓶的质量为_____(用含m1或m2的代数式表示)。
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取m克高锰酸钾、m克氯酸钾和m克氯酸钾(另加少量二氧化锰)分别加热,实验测得加热温度与产生氧气的关系如下图。下列分析正确的是( )
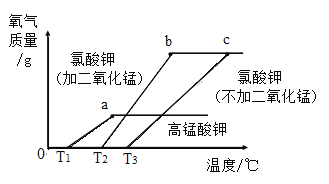
A.热稳定性:高锰酸钾>氯酸钾
B.a、b两点物质均为混合物,且含有一种相同的物质
C.加入适量二氧化锰可使氯酸钾产生氧气的反应速度变快,但并不增加氧气的量
D.氯酸钾中氧元素的含量(氧元素质量与物质质量之比)一定比高锰酸钾中氧元素含量高
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
①称取1.6g胆矾(CuSO4·5H2O)晶体,研细后加入10mL蒸馏水溶解。
②将足量的NaOH溶液与上述溶液充分反应生成蓝色沉淀,过滤后洗涤沉淀。
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变黑色,研细备用。
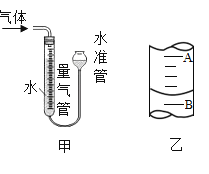
④按上表中的质量混合好固体后,在相同条件下加热试管并与(MnO2)的催化效果做比较,实验时间均以生成50mL气体为准(见图甲),其他可能影响实验甲乙的因素均忽略。回答下列问题:
编号 | 氯酸钾(KClO3)质量/g | 其他物质质量/g | 待测数据 |
1 | 2 | / | |
2 | 2 | 氧化铜(CuO)0.5 | |
3 | 2 | 二氧化锰(MnO2)0.5 |
(1)上述实验步骤中需要使用玻璃棒的是__________。(填序号)
(2)表格中“待测数据”是指________。
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意_________
a 视线与凹液面最低处相平
b 读数前不能移动量气管和水准管
c 保持水准管静止,待水准管中液面不再上升时,立刻读数
d 读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差lmL,刻度A为20,则此时气体的读数为___________。
(5)如果要进一步探究(CuO)在反应中是否起到催化作用,请完成后续实验。(提示:可从催化剂的概念完成实验)
实验步骤 | 设计这一步骤的目的 |
实验表明,加入氧化铜(CuO)后产生氧气(O2)的速率比未加入时快得多 | 氧化铜(CuO)能加快氯酸钾(KClO3)的分解 |
①___________ | ___________ |
②___________ | ___________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气是初中化学学习中非常重要的物质之一,小文同学在复习过程中对氧气的性质和用途进行了科学整理和归纳,并形成知识树如图所示。请你参考并回答相关问题:
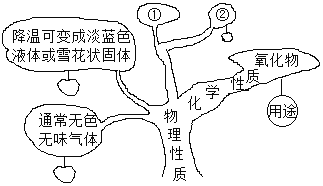
(1)在氧气物理性质的知识中已经给出两个实例,还有①②两方面,请你写出其中一条物理性质_____。
(2)在氧气化学性质中,铁、硫、碳等物质可以在氧气中燃烧。
①如图所示为铁丝在氧气中燃烧的改进实验,用适量过氧化氢溶液和二氧化锰代替原实验中集气瓶里的水。
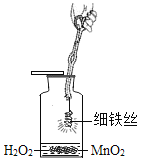
I.过氧化氢溶液加二氧化锰所发生化学反应的文字表达式为_____。
II.实验中观察到铁丝燃烧的现象是_____。写出该反应的文字表达式_____。
III.改进后实验和原实验相比优点是_____。
②做硫在氧气中燃烧实验时,集气瓶底部需放少量水,其作用是_____。
③做木炭在氧气中燃烧实验时为什么将木炭自上而下缓慢伸入盛有氧气的集气瓶_____。
④燃烧和缓慢氧化都有氧气参加。它们的共同点是_____。(填一点)
(3)物质性质决定物质用途,下列有关氧气的用途正确的是_____。(填序号)
A 做燃料 B 救治病人 C 炼钢 D 潜水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】木炭与孔雀石(主要成分是Cu2(OH)2CO3,杂质不参加反应,不含铜、氧、碳、氢元素)的混合物26.2g,隔绝空气加热至高温,恰好完全反应后得到固体(只有铜和杂质)质量为15.6g,混合物中的碳元素完全转化为二氧化碳,则孔雀石中铜元素的质量分数为( )
[提示: Cu2(OH)2CO3![]() 2CuO +CO2↑+H2O]
2CuO +CO2↑+H2O]
A.4.8%B.9.6%C.50%D.51.2%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究酸与碱之间的反应,进行下列实验活动:
(提出问题)酸与碱能否发生反应?
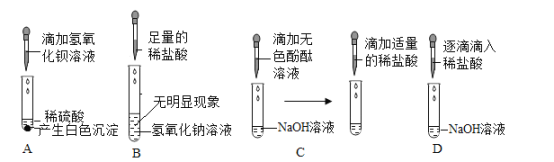
(实验与结论)秦思和石建分别选了不同的酸碱进行实验A、B。A中产生现象的原因是_____(用化学方程式解释),根据A中现象,秦思认为酸碱能发生反应。据B中现象,石建认为无法确定其中的酸碱能否反应。经思考讨论后,进行实验C,通过_____的现象,证明了_____(填一种离子的变化情况),进而证明了其中的酸与碱能发生反应。
(证据与解释)裘臻进行实验D,向氢氧化钠溶液中多次滴加稀盐酸,测定溶液pH,绘制溶液pH随加入的稀盐酸变化的曲线图E。得出与C相同的实验结论的依据是_____。
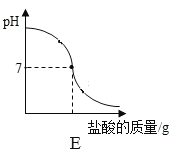
(反思与分析)实验A、C与D,通过不同的证据,都能证明酸与碱能发生反应。通过比较,崇湜发现从_____角度分析,实验A 中产生的白色沉淀不是酸与碱反应的实质。通过归纳,发现酸与碱反应的微观实质是_____。
(归纳提炼)通过上述实验可知,探究酸碱之间能否发生反应的实验设计思路是:通过明显现象,证明_____或_____。探究酸碱反应的实质的实验设计思路是:借助其他试剂或仪器,证明_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下,氯酸钾在水中溶解度(100 g水中的最大溶解量)较小,工业上可通过如下转化制得。
![]()
(1)实验室用氯酸钾制取氧气的化学方程式为_____。
(2)反应I中,通电时发生的反应为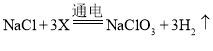 ,则X的化学式为_____。
,则X的化学式为_____。
(3)反应II的化学方程式为![]() ,反应中四种物质都由离子构成。请表示两个氯酸根离子_____。
,反应中四种物质都由离子构成。请表示两个氯酸根离子_____。
(4)该转化中可以循环利用的物质是_____(填名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取40克石灰石样品放在烧杯中,然后向其中逐滴加入稀盐酸,使之与稀盐酸充分反应(杂质不参与反应),恰好完全反应时,加入稀盐酸的质量为200克,反应后烧杯中物质的总质量为226.8克。请计算:
(1)反应生成二氧化碳的质量_________。
(2)石灰石样品中碳酸钙的质量分数_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com