
| 选项 | 物 质 | 操作方法 |
| A | Fe粉【Cu粉】 | 加入CuSO4溶液,过滤 |
| B | CaO粉末【CaCO3粉末】 | 加足量的水,充分搅拌后过滤 |
| C | CuSO4溶液【硫酸】 | 加入过量CuO粉末,加热,充分反应后过滤 |
| D | NaOH溶液【Ca(OH)2溶液】 | 通入过量CO2气体,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Fe粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、硫酸能与过量CuO粉末在加热条件下反应生成硫酸铜和水,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、Ca(OH)2溶液和NaOH溶液均能与CO2气体反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:选择题
 物质王国发生了一起团伙盗窃案,“警察”把三名“嫌疑犯”(分别是稀硫酸、氯化钠溶液和石灰水,如图)带回了“警察局”.上级派出下列四名“警察”分别去审问“他们”(即把“他们”鉴别出来).无法完成任务的“警察”是( )
物质王国发生了一起团伙盗窃案,“警察”把三名“嫌疑犯”(分别是稀硫酸、氯化钠溶液和石灰水,如图)带回了“警察局”.上级派出下列四名“警察”分别去审问“他们”(即把“他们”鉴别出来).无法完成任务的“警察”是( )| A. |  紫色石蕊试液“警察” | B. |  pH试纸“警察” | ||
| C. |  稀盐酸溶液“警察” | D. |  纯碱溶液“警察” |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化汞加热分解:HgO$\frac{\underline{\;\;△\;\;}}{\;}$Hg+O2↑ | |
| B. | 铁在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | |
| C. | 铁片投入稀盐酸中:2Fe+6HCl=2 FeCl3+3H2↑ | |
| D. | 碳在氧气中燃烧:C+O2=CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫酸盐 | B. | 碳酸盐 | C. | 二氧化碳 | D. | 硝酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2O2 | B. | HCl溶液 | C. | NaOH溶液 | D. | AgNO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | >7% | B. | 7.0% | C. | >8% | D. | 8.0% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④ | B. | ③⑤⑥ | C. | ②③⑥ | D. | ②⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
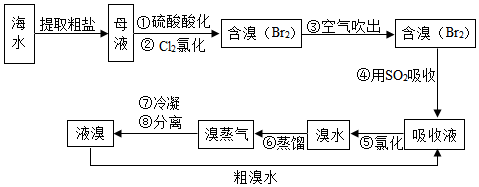
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com