
���� ��1��������Ȼ��ά���ص���������
��2������ʳƷ�и�����Ӫ�������������
��3�����ݻ���̿����������;��������
��4�������Ҵ�ȼ�գ����ɶ�����̼��ˮ�Լ��Ի�����Ӱ�����������
��� �⣺��1������T��������Ȼ��ά������ά����ˮ�Ժá����Ժá��������ʣ������ˮ�Ժã������Ժû��������ʣ���
��2���ƹ��и���ά���ء������и��������ʡ��������и�����֬�뵰���ʡ����и������ࣻ�������
��3������̿���������ԣ���������ȥˮ�е�ɫ������ζ�����������
��4���Ҵ��������ڵ�ȼ�������·�Ӧ���ɶ�����̼��ˮ���Ҵ���ȼ�Ͽ��Խ�Լʯ����Դ��ȼ������ˮ�Ͷ�����̼���Ի�������ȾС�����C2H5OH+3O2$\frac{\underline{\;��ȼ\;}}{\;}$2CO2+3H2O����Լʯ����Դ�������ڻ�������
���� �����ѶȲ���ͬѧ����ѧϰ������ѧ�����ѧ֪ʶ�����ܽ���ɣ������°빦�������ã����ղ��ϵ��ص㡢ʳƷ�и�����Ӫ���ء�����̿�������Լ���ѧ����ʽ��д�����������������ȷ�����Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ�Ӻ��������� | B�� | �������Ӻ��������� | ||
| C�� | ��ԭ�Ӻ���ԭ�� | D�� | ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ��; |
| A | ������֧��ȼ�� | ��ȼ�� |
| B | ������ѧ�����ȶ� | ��ʳƷ������ |
| C | ͭ�����õĵ����� | ������ |
| D | ����������ˮ��Ӧ | ��ʳƷ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| �¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
| �ܽ� ��/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A�� | 20��ʱ��20g KNO3���뵽50gˮ�У��ܵõ�65.8g��Һ | |
| B�� | KNO3���ܽ�ȱ�NaCl���ܽ�ȴ� | |
| C�� | 60��ʱ��210g KNO3������Һ������20�棬��Һ������Ϊ131.6g | |
| D�� | 20��ʱ��40g NaCl���뵽100gˮ�У���������60����γɲ�������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
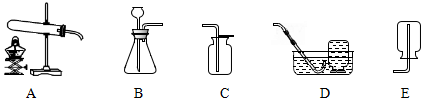
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
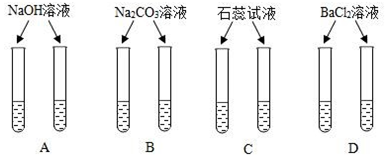
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��ʾ��С�Թ���ʢ��ˮ��U��������ˮ���ƽ�����Թ��м���ij���ʺ�U������ˮ������Ҹߣ������ӵ����ʿ����ǣ�������
��ͼ��ʾ��С�Թ���ʢ��ˮ��U��������ˮ���ƽ�����Թ��м���ij���ʺ�U������ˮ������Ҹߣ������ӵ����ʿ����ǣ�������| A�� | ϡ���� | B�� | NaOH���� | C�� | ϡH2SO4 | D�� | NaCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��pH��С | B�� | ��Һ��������ǿ | ||
| C�� | ��������������С | D�� | ��Һ��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com