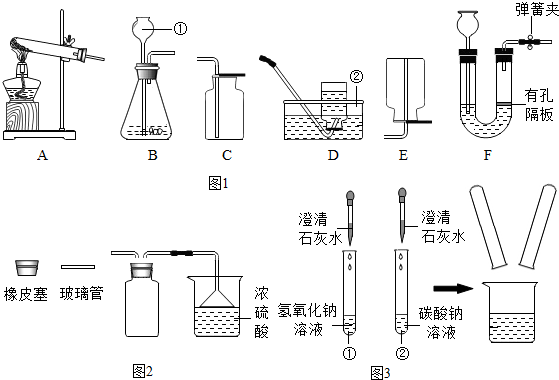
(2013?清城区模拟)如图1所示,请根据下列装置,回答问题:
(1)写出标号①、②的仪器名称:①
长颈漏斗
长颈漏斗
,②
水槽
水槽
.
(2)实验室制取CO
2的反应方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;检验二氧化碳气体的反应原理是
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
(用化学方程式表示).
(3)实验中为了回收二氧化锰固体.正确操作的先后顺序是
BCDA
BCDA
(填写选项序号).
A.烘干 B.溶解 C.过滤 D.洗涤
(4)在实验室制取CO
2的实验装置中,F装置相对于B装置具有的优点是
可以控制反应的随时发生或停止
可以控制反应的随时发生或停止
.
(5)实验室通过加热固体氯化铵和固体氢氧化钙的混合物反应可以得到NH
3(极易溶于水,密度比空气小),你将选择图2中的
E
E
作为实验室收集NH
3的装置.
(6)图3是收集NH
3并对尾气进行处理的装置(浓硫酸可与NH
3反应生成硫酸铵),请根据图示把装置画完整.
(7)图3中倒扣漏斗倒放的作用是
防止倒吸
防止倒吸
.


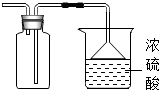
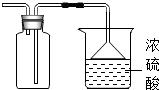 装置图如右图:
装置图如右图:
