
| A. | 块状石灰石与稀硫酸反应,持续产生气泡 | |
| B. | 铜丝在空气中加热,生成黑色的氧化铜 | |
| C. | 聚乙烯在空气中灼烧,无刺激性气味气体 | |
| D. | 铁锈加入稀盐酸中,得到浅绿色溶液 |
分析 A、根据石灰石与稀硫酸反应的实验现象,进行分析判断.
B、根据铜丝在空气中加热的实验现象,进行分析判断.
C、根据聚乙烯在空气中灼烧的现象,进行分析判断.
D、根据酸的化学性质,进行分析判断.
解答 解:A、稀硫酸与块状石灰石反应生成微溶于水的硫酸钙,会覆盖在石灰石表面,阻止反应的进行,不能持续产生气泡,故选项说法错误.
B、铜丝在空气中加热,生成黑色的氧化铜,是实验结论而不是实验现象,故选项说法错误.
C、聚乙烯在空气中灼烧,无刺激性气味气体,故选项说法正确.
D、铁锈加入稀盐酸中,得到黄色溶液,故选项说法错误.
故选:C.
点评 本题难度不大,掌握碱的化学性质、常见物质燃烧的现象、酸的化学性质即可正确解答,在描述实验现象时,需要注意实验结论和实验现象的区别.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. |  我是常见金属中最活泼的 | B. |  我能供给呼吸和支持燃烧 | ||
| C. |  我是常见气体中密度最小的 | D. |  剧毒的我,小心呼吸中毒 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
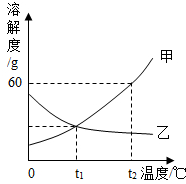 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
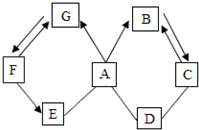 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同的气体,D是一种红棕色粉末,E常用于改良酸性土壤,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同的气体,D是一种红棕色粉末,E常用于改良酸性土壤,F是相对分子质量最小的氧化物.请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
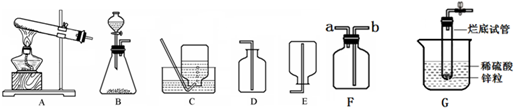
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 第一组 | 第二组 | 第三组 | 第四组 | 第五组 | |
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80℃ |
| 溶质种类 | 食盐 | 食盐 | 食盐 | 硝酸钾 | 食盐 |
| 溶质状态 | 粉末 | 粉末 | 块状 | 粉末 | 粉末 |
| 溶质质量 | 3.6g | 3.6g | 3.6g | 3.6g | 3.6g |
| 溶剂种类 | 水 | 植物油 | b | 水 | 水 |
| 溶剂质量 | 10g | a | 10g | 10g | 10g |
| 溶解情况 | 固体全溶 | 固体不溶 | 固体全溶 | 固体部分溶 | 固体全溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
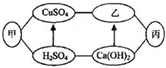 下图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).
下图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 (1)2016年底,沪昆高铁和云贵高铁即将开通,人们的出行将更加方便、快捷.结合所学化学知识,回答下列问题:
(1)2016年底,沪昆高铁和云贵高铁即将开通,人们的出行将更加方便、快捷.结合所学化学知识,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com