
 氯化钙钾石的化学式为KCl•xCaC12(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:
氯化钙钾石的化学式为KCl•xCaC12(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:分析 由图可以看出,当加入106g碳酸钠溶液时生成10g沉淀,根据碳酸钙的质量和对应的化学方程式可求氯化钙的质量和碳酸钠的质量,进而求算对应的质量分数.
解答 解:图中B点时碳酸钠已经不过,此时的溶质为原样品中的氯化钾,生成的氯化钠和过量的碳酸钠.
设样品中的氯化钙的质量为x,参加反应的碳酸钠的质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100
y x 10g
$\frac{106}{y}$=$\frac{111}{x}$=$\frac{100}{10g}$
x=11.1g
y=10.6g
则18.55g氯化钙钾石样品中,氯化钾的质量18.55g-11.1g=7.45g
所含钾元素的质量为7.45g×$\frac{39}{39+35.5}$×100%=3.9g
18.55g氯化钙钾石样品中,钾元素的质量分数为$\frac{3.9g}{18.55g}$×100%≈21.0%
所用Na2CO3溶液中溶质的质量分数为$\frac{10.6g}{106g}$×100%=10%
故答案为:(1)氯化钾、氯化钠以及碳酸钠.(化学式也可)
(2)21.0%(21%也可).
(3)10%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
| A. | 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 | |
| B. | 水和过氧化氢的组成元素相同,则两者的化学性质相同 | |
| C. | 化合物由不同种元素组成,则只含有一种元素的物质一定不是化合物 | |
| D. | 洗洁精清洗油污利用了乳化作用,则汽油清洗油污也是利用了乳化作用 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 2012年4月15日,央视《每周质量报告》曝光一些企业用生石灰处理皮革废料熬制工业明胶,制成药用胶囊,最终进入消费者腹中.工业明胶,是一种淡黄色或棕色的碎粒,无不适气味,无肉眼可见杂质.其分子量为1-10万,水分和无机盐含量在16%以下,蛋白质含量在82%以上,是一种理想的蛋白源.
2012年4月15日,央视《每周质量报告》曝光一些企业用生石灰处理皮革废料熬制工业明胶,制成药用胶囊,最终进入消费者腹中.工业明胶,是一种淡黄色或棕色的碎粒,无不适气味,无肉眼可见杂质.其分子量为1-10万,水分和无机盐含量在16%以下,蛋白质含量在82%以上,是一种理想的蛋白源.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 试管号 | 0.5%淀粉溶液 | 0.5%HCl溶液 | 蒸馏水 | 稀释的唾液 |
| 1 | 2mL | 0 | 1mL | 1mL |
| 2 | 2mL | 1mL | 0 | 1mL |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
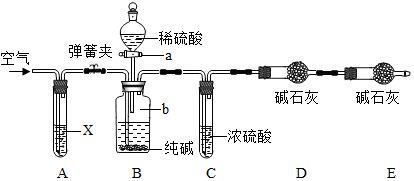
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
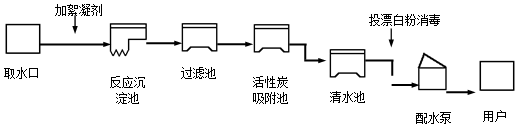
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
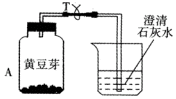 小明为了探究植物也能呼吸,做了以下实验:把装有吸干外表水的黄豆芽的塑料瓶A放在暗处24小时;导管T处用夹子夹住,不让外界空气进入;24小时后,观察塑料瓶壁;把T处夹子打开,用力压A瓶,让瓶内气体通入到右侧烧杯内,发现澄清石灰水变浑浊,塑料瓶内壁有水珠,用温度 计测量豆芽温度,可发现温度升高.
小明为了探究植物也能呼吸,做了以下实验:把装有吸干外表水的黄豆芽的塑料瓶A放在暗处24小时;导管T处用夹子夹住,不让外界空气进入;24小时后,观察塑料瓶壁;把T处夹子打开,用力压A瓶,让瓶内气体通入到右侧烧杯内,发现澄清石灰水变浑浊,塑料瓶内壁有水珠,用温度 计测量豆芽温度,可发现温度升高.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
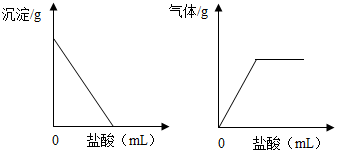 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )| A. | 肯定只存在Na2CO3 | B. | 肯定不存在BaCl2 | ||
| C. | 可能存在Na2SO4 | D. | 可能存在NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com