
 2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |
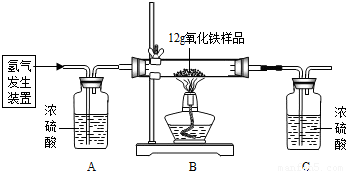
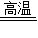 2Fe+3H2O
2Fe+3H2O
 ×100%≈66.7%
×100%≈66.7%

 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:
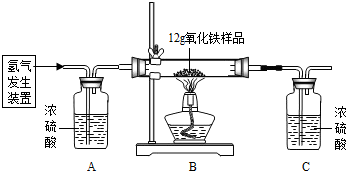 (2012?青岛)某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3
(2012?青岛)某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3
| ||
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
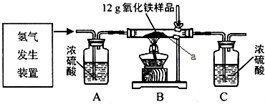 某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:氢气和氧化铁在高温条件下发生置换反应,杂质不参加反应,浓硫酸具有吸水性,假定每步均完全反应或吸收).
某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:氢气和氧化铁在高温条件下发生置换反应,杂质不参加反应,浓硫酸具有吸水性,假定每步均完全反应或吸收).| 装置B | 装置C | |
| 反应前的质量/g | 86.3 | 286.9 |
| 反应后的质量/g | 83.9 | 284.2 |
查看答案和解析>>
科目:初中化学 来源:山东省中考真题 题型:计算题
某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3 2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题: 2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题: | |||||||||
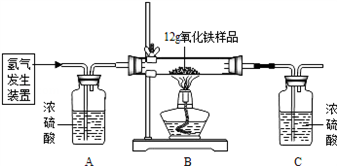 | |||||||||
得到如下数据:
| |||||||||
| (1)请计算样品中氧化铁的质量分数.(写出计算步骤,计算结果精确到0.1%) (2)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为____________(不用化简);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会___________(选填“偏大”、“偏小”或“不变”). |
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3===2Fe+3H2O
杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:

(1)请计算样品中氧化铁的质量分数。(写出计算步骤,计算结果精确到0.l%)
(2)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_________________________________________________(不用化简);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com