已知有如下反应:A+B→C+D.(答题时需注明必要的反应条件)
(1)若A为Al、B为FeSO4(溶液),则反应的方程式为 .
(2)若A为SO2,写出一个可能的化学方程式 .
(3)若A为CO2、B为H2O,则反应的方程式为 .
(4)若反应为A+2NaOH═2C+Cu(OH)2↓,则A的化学式可能为 .(写一种)
【答案】
分析:(1)铝的金属活动性比铁的强,故铝能把硫酸亚铁中的铁置换出来,发生的反应为置换反应;
(2)若A为SO
2,则B为可溶性的碱溶液,如氢氧化钠溶液、氢氧化钡溶液、氢氧化钾溶液等;
(3)若A为CO
2、B为H
2O,又因为发生A+B→C+D,所以发生光合作用的化学方程式;
(4)若反应为A+2NaOH═2C+Cu(OH)
2↓,A与碱反应生成氢氧化铜沉淀,故A为可溶性的铜的盐.
解答:解:(1)由题意,若A为Al、B为FeSO
4(溶液),又因为发生A+B→C+D,故2Al+3FeSO
4=Al
2(SO
4)
3+3Fe;
(2)若A为SO
2,则B为可溶性的碱溶液,故SO
2+2NaOH=Na
2SO
3+H
2O;
(3)若A为CO
2、B为H
2O,又因为发生A+B→C+D,故6CO
2+6H
2O
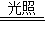
C
6H
12O
6+6O
2;
(4)A与碱反应生成氢氧化铜沉淀,故A为可溶性的铜的盐,故A可能为氯化铜、硝酸铜.
故答为:(1)2Al+3FeSO
4=Al
2(SO
4)
3+3Fe;
(2)SO
2+2NaOH=Na
2SO
3+H
2O (合理即可);
(3)6CO
2+6H
2O
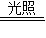
C
6H
12O
6+6O
2;
(4)CuCl
2[或Cu(NO
3)
2]
点评:解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征及结构特征),导出结论,最后别忘了把结论代入原题中验证,若“路”走得通则已经成功.

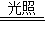 C6H12O6+6O2;
C6H12O6+6O2;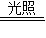 C6H12O6+6O2;
C6H12O6+6O2;

 阅读快车系列答案
阅读快车系列答案