
分析 (1)若C为厨房内常用的调味品,则C为氯化钠;在A溶液中加入铁粉能产生氢气,结合铁能与酸反应生成氢气,则A为酸;A与B反应生成氯化钠和D,则A为稀盐酸,稀盐酸能与氢氧化钠溶液反应生成氯化钠和水,进行分析解答.
(2)若A的固体是一种干燥剂,C是蓝色沉淀,C为氢氧化铜沉淀,结合氢氧化钠固体与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,据此进行分析解答.
解答 解:(1)若C为厨房内常用的调味品,则C为氯化钠;在A溶液中加入铁粉能产生氢气,结合铁能与酸反应生成氢气,则A为酸;A与B反应生成氯化钠和D,则A为稀盐酸,稀盐酸能与氢氧化钠溶液反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH═NaCl+H2O.
(2)若A的固体是一种干燥剂,C是蓝色沉淀,C为氢氧化铜沉淀,结合氢氧化钠固体与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,则A为氢氧化钠,反应的化学方程式为:.
故答案为:(1)稀盐酸;HCl+NaOH═NaCl+H2O;
(2)氢氧化钠;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题
 氧是地壳中含量最多的元素,氧及其化合物是化学学习和研究的重要内容.
氧是地壳中含量最多的元素,氧及其化合物是化学学习和研究的重要内容.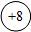 表示原子核,带8个单位正电荷
表示原子核,带8个单位正电荷查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
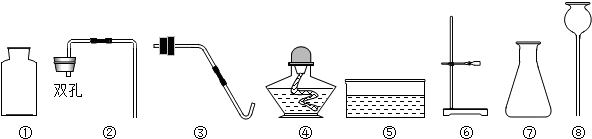
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用肥皂水鉴别硬水和软水 | |
| B. | 用水鉴别氢氧化钠固体和硝酸铵固体 | |
| C. | 用点燃闻气味的方法鉴别羊毛和合成纤维 | |
| D. | 用酚酞溶液鉴别碳酸钠溶液和氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com