
【题目】铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(1)合金中铜、镁的质量比.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
【答案】(1)33︰17 (2)10.5%
【解析】本题考查有关化学方程式的计算.由题意分析可得到第4次实验完成后,剩余的固体全是铜,其质量为13.2g,那么镁的质量为:20g-13.2g=6.8g.求稀硫酸的溶质质量分数根据第一次实验代入化学方程式就可以求出.
(1)剩余固体的质量为铜的质量,所以铜的质量为13.2g,金属镁的质量=20g-13.2g=6.8g,合金中铜、镁的质量比=13.2︰6.8=33︰17.
(2)分析表中数据可知,与70g稀硫酸完全反应消耗镁的质量为1.8g.
设与1.8g金属镁反应的稀硫酸的溶质的质量为x.
Mg+H2SO4=MgSO4+H2↑
24 98
1.8g x
![]()
x=7.35g
所加稀硫酸的溶质的质量分数![]()
答:所加稀硫酸的溶质的质量分数为10.5%.


科目:初中化学 来源: 题型:
【题目】2012年9月25日,我国第一艘航空母舰“辽宁号”正式入列.这对我国捍卫国家主权,维护领土完整具有重要意义,下图为“辽宁号”实物图,请回答问题.

(1)图中表示的物质由金属材料制成的是________.
(2)航母外壳使用的是特种钢,特种钢属于________(选填“纯净物”或“混合物”).
(3)特种钢在海水中特别耐腐蚀.请你写出生活中一种防止铁制品锈蚀的方法:________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图是氯化钠和硝酸钾两种固体物质的溶解度曲线.
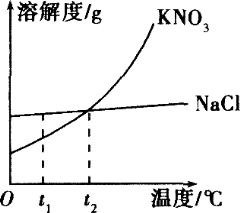
某兴趣小组为了研究NaCl和KNO3的溶解和结晶,做了两组实验(室温下),其过程如下:
[第一组]

[第二组]
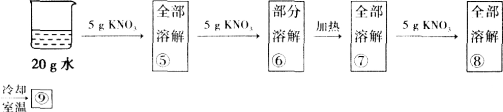
(1)①中溶质的质量分数为________________,⑨的现象是________________.
(2)第一组实验中操作a为________,所得氯化钠固体质量增多可能是下列原因中的(填字母序号)________.
A.溶解NaCl固体时,没有用玻璃棒搅拌
B.称量5g NaCl固体后,称量纸上仍留有固体
C.蒸发时,未及时停止加热,有固体溅出
D.蒸发后所得NaCl固体中仍含有水分
(3)上述实验过程中一定属于饱和溶液的是(填数字序号,下同)________,溶质与溶剂质量比一定相等的是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对下列各符号中“3”所表示的含义,其说法不正确的是
A.3H——表示三个氢原子
B.3H2O——表示三个水分子
C.Al3+——表示铝元素的化合价为+3
D.SO3——表示一个三氧化硫分子中含有三个氧原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】配制50g一定溶质质量分数的氯化钠溶液,实验步骤如下:
(1)计算:氯化钠质量和水的体积(水的密度:1.0g/mL).
(2)称量:如图所示(右盘无砝码)称量的氯化钠质量为________g.
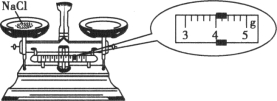
量取:选择________(填“30”“50”或“100”)mL的量筒准确量取________水.
(3)溶解:把氯化钠和水全部转移到烧杯中,搅拌至氯化钠全部溶解,配得的氯化钠溶液中溶质的质量分数为________.
(4)装瓶、贴标签:请填写图所示标签.

【反思】
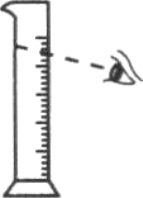
(5)上述实验过程中,用量筒量取水时,若按图方式进行读数,将导致所配溶液的溶质质量分数________(填“偏大”“不变”或“偏小”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上采用离子交换膜电解槽电解饱和食盐水,可以得到高浓度的烧碱溶液(含NaOH35%~48%).某学习小组为了验证附近氯碱化工厂产生的NaOH溶液是否达到高浓度标准,进行了如下操作,请你参与计算:
(1)到工厂采集了电解槽中的NaOH溶液100g.NaOH中氧元素的质量分数是________.
(2)在实验室用如图所示浓硫酸配制200g 24.5%的稀硫酸,计算所取浓硫酸的体积(计算结果取整数).

(3)进行中和测定,向采集到的溶液中逐渐加入所配制的稀硫酸,并不断测定溶液的pH,当pH=7时,消耗稀硫酸160g.通过计算判断此时电解槽中NaOH溶液是否达到高浓度标准.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】12.8g氧化铁和氧化铜的混合物,与足量的一氧化碳充分反应后,固体物质的质量减少3.2g,则原混合物中氧化铁和氧化铜的质量比为( )
A.3︰2
B.2︰1
C.3︰1
D.1︰1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示(→表示转化关系,—表示相互之间会反应)。己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是生活中最常见的溶剂,且与B的物质类别相同,都是氧化物。(部分反应物、生成物及反应条件己略去)
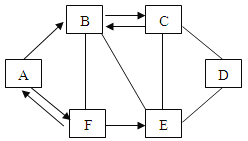
请回答:
(1)写出A、B、F的化学式:A______,B______,F______.
(2)F转化为E的反应化学方程式是 ;
写出E物质的一种用途 ;
(3)C与D的反应化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com