
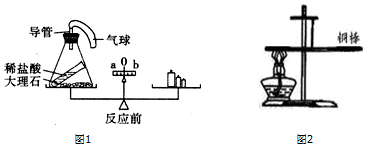
分析 (1)结合物理知识,从气球膨胀会产生一定的浮力的角度分析,会造成左侧质量减小,使天平的指针向右偏转.
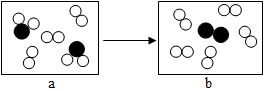
(2)依据质量守恒定律的内容分析产物的质量大于镁条的质量,依据反应时氧化镁以白烟的形式扩散到空气中分析m1>m2的原因.
(3)根据锌和稀硫酸反应放热进行分析.
(4)铜与氧气反应生成了氧化铜,所以可以判断在加热前后铜棒不能再保持平衡,可以据此解答该题.
解答 解:(1)该反应中大理石和盐酸反应生成了二氧化碳气体,生成的气体使气球膨胀,膨胀的气球会产生一定的浮力,造成左侧质量减小,指针向右偏转;
(2)根据质量守恒定律,生成氧化镁的质量=参加反应的镁的质量+氧气的质量,所以m1小于m2;镁带燃烧时放出耀眼的白光,放出大量的热,放出大量的白烟,仔细观察会发现:白烟有很大一部分向上,生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中导致m1>m2.
(3)锌和稀硫酸反应放热,反应结束后试管中剩余锌粒呈黑色.
(4)左端的铜在加热的条件下与氧气反应生成了氧化铜,反应的化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
所以可以判断在加热前后铜棒不能再保持平衡.由于氧气参与反应,所以反应后固体质量增加,本实验现象与质量守恒定律不矛盾.
故答案为:(1)b;左边反应生成二氧化碳气体,使气球膨胀,增大了浮力,造成向b方向偏转;
(2)<;生成物氧化镁部分以白烟的形式扩散到空气中;
(3)放热;黑;
(4)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;不能;没有.
点评 本题主要考查了对实验产生的各种情况的综合分析,结合物理知识,难度不大,开放性强,要求同学们思维开放,综合运用所学知识.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:填空题
 (1)N(NO2)3 是科学家2011年发现的一种新型火箭燃料,其中氮元素和氧元素的质量比为7:12.
(1)N(NO2)3 是科学家2011年发现的一种新型火箭燃料,其中氮元素和氧元素的质量比为7:12.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
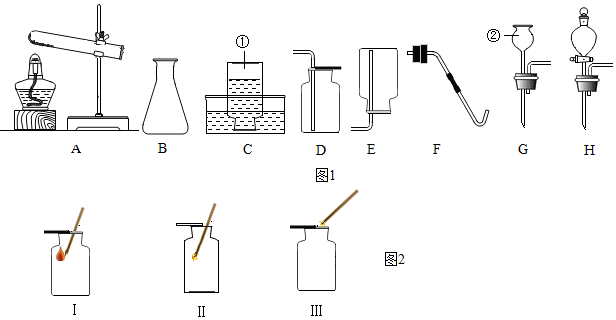
 某化学小组同学用如图装置制取一定量的氧气.请你参与探究:
某化学小组同学用如图装置制取一定量的氧气.请你参与探究:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
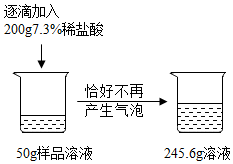 实验室有一瓶放置已久的氢氧化钠溶液,为探究其变质情况,某化学兴趣小组进行了以下探究.
实验室有一瓶放置已久的氢氧化钠溶液,为探究其变质情况,某化学兴趣小组进行了以下探究.| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量该溶液与试管中,加入足量稀盐酸 | 有气泡冒出 | 氢氧化钠溶液一定变质了 |
| (2)另取少量该溶液与试管中,加入氯化钙(或CaCl2). | 有白色沉淀生成 | 猜想2正确 |
| (3)取步骤(2)试管中的少量上层清液,加入酚酞试液 | 溶液变成红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝和铜丝分别插入稀硫酸中 | B. | 铜丝插入硫酸亚铁溶液中 | ||
| C. | 铁丝和铜丝分别在氧气中点燃 | D. | 铁丝和铜丝分别插入硫酸锌溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com