
二氧化硫是造成酸雨的主要气体,其溶于水形成的水溶液叫亚硫酸(H2SO3)。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H2S+H2SO3 ===3S↓+3H2O。下列亚硫酸溶液的pH随通入的硫化氢体积变化曲线示意图中,正确的是

A. A B. B C. C D. D
C 【解析】亚硫酸溶液显酸性,pH<7,通入硫化氢气体后,硫化氢与亚硫酸反应生成硫单质和水,使溶液的pH增大,当恰好反应时,pH=7,硫化氢气体易溶于水,继续通入硫化氢气体,溶液呈酸性,pH<7,但由于氢硫酸的酸性弱于亚硫酸,所以溶液最后的pH值会比开始时大,故C项正确。 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源:黑龙江省大庆市杜尔伯特县2018届九年级(初四)下学期期中考试化学试卷 题型:单选题
配制10%的氯化钠溶液时,不会引起溶液中氯化钠的质量分数偏小的是
A.用量筒量取水时仰视读数 B.配制溶液的烧杯用少量蒸馏水润洗
C.氯化钠晶体不纯 D.转移已配好的溶液时,有少量溶液溅出
D 【解析】A、量取液体时仰视,视线低于凹液面和刻度线,因此所读取的数值小于液体的实际体积;结果会造成溶剂水的量偏大而引起质量分数偏小.不符合要求,故不选A; B、用水润洗烧杯时,烧杯壁残留的水使所得溶液中溶剂水的量偏大,造成质量分数偏小.不符合要求,故不选B; C、称取的氯化钠固体不纯,致使溶质质量小于配制所需要的溶质质量,引起质量分数偏小.不符合要求,故不选C; D、已...查看答案和解析>>
科目:初中化学 来源:江苏省常熟市2018届九年级下学期适应性质量检测化学试卷 题型:单选题
除去下列物质中的少量杂质,所选试剂及操作都比较合理的是
选项 | 物质 | 杂质 | 试剂和操作方法 |
A | 氯化钠 | 碳酸钠 | 加过量的稀盐酸,蒸发结晶 |
B | 氨气 | 水 | 将混合气体通过浓硫酸 |
C | 氯化钾 | 氯化镁 | 加适量的氢氧化钾溶液,过滤、洗涤、干燥 |
D | 硫酸铜 | 硫酸 | 加适量铜粉 |
A. A B. B C. C D. D
A 【解析】A、碳酸钠能与过量的稀盐酸反应生成氯化钠、水和二氧化碳,再蒸发,结晶,能除去杂质且没有引入新的杂质,符合除杂原则,正确;B、浓硫酸具有吸水性,但能与氮气反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,错误;C、氯化镁能与适量氢氧化钾溶液反应生成氢氧化镁沉淀和氯化钾,过滤即可除去沉淀,不需要洗涤和干燥,不符合除杂原则,错误;D、铜粉与硫酸铜和硫酸都不反应,不能除杂,错误。...查看答案和解析>>
科目:初中化学 来源:江苏省常熟市2018届九年级下学期适应性质量检测化学试卷 题型:单选题
下列有关物质的名称、俗名、化学式中,三者皆指同一物质的是
A. 氯化氢、盐酸、HCl B. 氧化钙、生石灰、CaO
C. 碳酸钙、消石灰、CaCO3 D. 碳酸钠、小苏打、Na2CO3
B 【解析】A、氯化氢的水溶液才叫盐酸,错误; B、氧化钙的俗称是生石灰,化学式为CaO,正确; C、碳酸钙是石灰石,消石灰是氢氧化钙,错误; D、碳酸钠是苏打,小苏打是碳酸氢钠,错误。故选B。查看答案和解析>>
科目:初中化学 来源:内蒙古乌拉特前旗2018届九年级第一模拟考试化学试卷 题型:简答题
下列是初中化学中的一些常见实验,请回答相关问题。
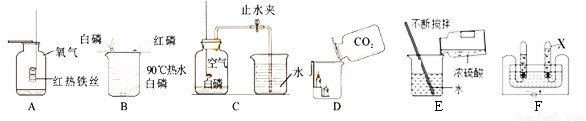
(1)A中的实验现象是_______________________;
(2)从B实验能得出燃烧条件之一是______________;
(3)C实验测定空气中氧气含量过程中,导致实验结果偏小的原因可能是_________(写一点)。
(4)通过D实验对CO2气体从物理性质和化学性质两个方面得到结论:物理性质___________(填一条即可),化学性质__________________(填一条即可)。
(5)E实验浓硫酸的稀释实验中,用玻璃棒搅拌的目的___________。
(6)F电解水实验中,在水中加入硫酸钠的作用是__________,X管中产生的气体是_______。
剧烈燃烧、火星四射、生成黑色固体。同时放出大量的热 可燃物必须与氧气接触(或温度达到着火点) 红磷量不足(合理即可) 密度比空气大 不能燃烧(不能支持燃烧) 搅拌使热量散失 增强水的导电性 氧气 【解析】本题考查了燃烧的条件探究,空气组成的测定,氧气的化学性质;二氧化碳的性质,浓硫酸的稀释,水的电解实验等。 (1)铁丝在氧气中剧烈燃烧、火星四射、生成黑色固体。同时放出大量的热; ...查看答案和解析>>
科目:初中化学 来源:内蒙古乌拉特前旗2018届九年级第一模拟考试化学试卷 题型:单选题
分析推理是化学学习中常用的思维方法。下列分析推理正确的是 ( )
A. 碱溶液pH大于7,所以pH大于7的溶液一定是碱溶液
B. 酸和碱作用生成盐和水的反应是中和反应,所以生成盐和水的反应一定是中和反应
C. 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
D. 单质是由同种元素组成的,所以由同种元素组成的纯净物一定是单质
D 【解析】A. 碱溶液pH大于7,但是pH大于7的溶液不一定是碱溶液,比如碳酸钠溶液显碱性,错误; B. 酸和碱作用生成盐和水的反应是中和反应,但是生成盐和水的反应不一定一定是中和反应,比如酸与金属氧化物反应生成盐和水不是中和反应,错误; C. 溶液中有晶体析出时,溶质质量减小,当溶液中有晶体析出时,可能是由于水分蒸发,所以溶质的质量分数可能增加,错误; D. 单质是由同...查看答案和解析>>
科目:初中化学 来源:安徽省合肥市育英学校2018届九年级中考模拟化学试卷 题型:计算题
下图是某药厂生产的一种抗酸药(治疗胃酸过多的药物)的说明书的部分内容.阅读后回答下列问题.
说明书
主要成分:碳酸氢钠(NaHCO3)
适 应 症:用于缓解胃酸(含有
盐酸)过多引起的胃痛
用 法:嚼碎后服用
规 格:2.5g/片
注意事项:胃溃疡患者慎服
现取4片药片碾碎后,加到烧杯中,再往烧杯中加入60g稀盐酸,完全反应后,烧杯中物质的总质量为65.6g,(药品的其它成分不溶于水,也不参加反应),求:
(1)生成二氧化碳的质量是___________.
(2)此药片中碳酸氢钠的质量分数是__________.
4.4g 84% 【解析】【解析】 (1)生成二氧化碳的质量:60g+2.5g/片×4片﹣65.6g═4.4g (2)设4片药片中碳酸氢钠的质量为x NaHCO3+HCl═NaCl+H2O+CO2↑ 84 44 x 4.4g x=8.4g 碳酸氢钠的质量分数为=×100%=84% 答:生成二氧化碳的质量是4.4g;碳酸氢钠的质量分数为84%。 ...查看答案和解析>>
科目:初中化学 来源:广东省江门市2018届九年级下学期第二次模拟考试化学试卷 题型:综合题
维生素C又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏,人体缺乏维生素C可能引发多种疾病,它的化学式是C6H8O6.计算:

(1)维生素C中含有_____种元素,
(2)维生素C中氢元素的质量分数为______(结果保留一位小数);
(3)小婷遵医嘱,她一天补充到的维生素C为_______mg;
(4)取一片“维生素C”溶于水,滴入紫色石蕊试液变红色,说明“V﹣C”的溶液显_______性.加热该溶液至沸腾,红色消失,所以在烹调新鲜蔬菜时要减少“V﹣C”的损失,应采取的措施可以是________________。
三; 4.5%; 20; 酸; 凉拌或避免高温加热; 【解析】(1)由维生素C的化学式C6H8O6可知,其中含有碳元素、氢元素和氧元素等三种元素; (2)维生素C的相对分子质量为:(12×6)+(1×8)+(16×6)=176;氢元素的质量分数为:×100%=4.5%; (3)根据医嘱,小婷一天应该吃2片维生素C药片,补充的维生素C的质量为:100mg×2×10%=20mg; ...查看答案和解析>>
科目:初中化学 来源:山东省潍坊市寿光、高密市2018届初三一模化学试卷 题型:科学探究题
小苏打(NaHCO3)和食盐(NaCl)是厨房中常用物质。现有一包白色固体,可能由NaHCO3和NaCl中的一种或两种组成。某科学小组同学展开了系列拓展性研究。
(一)定性分析
【实验目的】确定白色固体的组成
【实验方案】
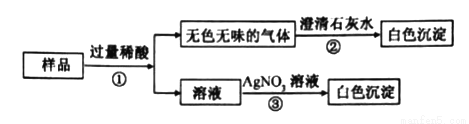
【实验结论】该白色固体由NaHCO3和NaCl两种物质组成
(1)基于上述实验结论,则步骤①中加入的过量稀酸应该是 。
(2)写出步骤②中生成白色沉淀的化学反应方程式 。
(二)定量分析
【实验目的】测定该白色固体中NaHCO3的质量分数
为了测定该样品中NaHCO3的质量分数,小吕、小周分别取a克该样品,设计了如下方案:
小吕方案Ⅰ:利用NaHCO3与稀硫酸反应产生CO2,通过测定生成CO2的质量,计算样品中NaHCO3的质量分数。
(3)小吕用下列装置完成本实验,装置的连接顺序是 (填装置的字母编号,装置不重复使用);
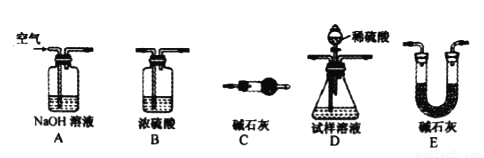
(4)D装置中的反应完全后,需再次通入空气,其目的是 。
小周方案Ⅱ:小周用沉淀法测定样品中NaHCO3的质量分数。操作流程如下:
(已知:NaHCO3+NaOH=Na2CO3+H2O)
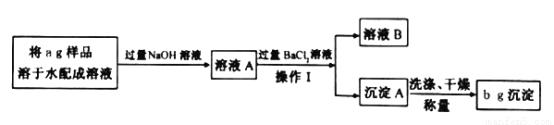
(5)为使定量分析更准确,在操作Ⅰ之前,需判断所加BaCl2溶液是否过量,请你设计一个合理方案: 。
(1)硝酸 (2)CO2+Ca(OH)2=CaCO3↓+H2O (3)ADBEC或ADBCE (4)把生成的二氧化碳全部排入装置E(或C)中,使之充分被吸收 (5)待浊液澄清后,继续滴加BaCl2溶液,若无沉淀产生则说明BaCl2已过量 【解析】(1)【实验结论】该白色固体由NaHCO3和NaCl两种物质组成,另溶液中加入硝酸银溶液后生成白色沉淀且沉淀不溶解,则沉淀为...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com