
分析 (1)氢氧化铝能与胃液中的盐酸反应生成氯化铝和水,写出反应的化学方程式即可.
(2)纯碱或小苏打等碱性物质与乳酸等有机酸反应生成二氧化碳气体.
(3)生石灰与水反应生成氢氧化钙,写出反应的化学方程式即可.
(4)考虑二氧化碳和氢氧化钙反应生成碳酸钙和水;
(5)铁锈的主要成分水氧化铁,氧化铁和稀盐酸反应生成氯化铁和水.
解答 解:(1)氢氧化铝能与胃液中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
(2)做馒头发酵面团时,会产生乳酸等有机酸,蒸馒头前需加进适量的纯碱或小苏打等碱性物质,故纯碱或小苏打等碱性物质与乳酸等有机酸反应生成二氧化碳气体,使蒸出的馒头疏松多孔;若加入的碱性物质过多,可向面团或蒸锅中滴加少许含H2CO3(填化学式)的酸性调味料,否则蒸出的馒头会变涩,颜色发黄.
(3)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.
(4)二氧化碳和石灰乳氢氧化钙反应的化学方程式为:CO2+Ca(OH)2═CaCO3+H2O;
(5)铁锈氧化铁和稀盐酸反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
故答案为:
(1)Al(OH)3+3HCl═AlCl3+3H2O;(2)CO2;H2CO3;(3)CaO+H2O═Ca(OH)2.
(4)CO2+Ca(OH)2═CaCO3+H2O;(5)Fe2O3+6HCl═2FeCl3+3H2O.
点评 本题难度不大,掌握中和反应应用、盐的化学性质与用途、生石灰的化学性质、化学方程式的书写是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | B. | 6HCl+2Fe=2FeCl3+3H2↑ | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | 2KClO3=2KCl+3O2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 从铝土矿(主要成分是Al2O3)中提炼金属铝 | |
| B. | 秸秆、杂草、粪便等在沼气池中发酵 | |
| C. | 二氧化碳气体经加压、降温得到干冰 | |
| D. | 一氧化碳燃烧生成二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲可能是Na2SO4,乙一定是H2SO4 | B. | 乙可能是H2SO4,丙一定是NaOH | ||
| C. | 甲可能是NaHSO4,丙一定是NaOH | D. | 乙可能是H2SO4,丁一定是H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
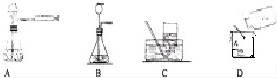
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 物质(括号内为杂质) | 除杂试剂 | 分离方法 |
| A | 二氧化锰粉末(碳粉) | 水 | 过滤 |
| B | 氯化铜溶液(氯化锌) | 金属铜 | 过滤 |
| C | 二氧化碳(一氧化碳) | 氢氧化钠溶液 | 洗气 |
| D | 氯化钠固体(碳酸钠) | 稀盐酸 | 蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com