
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 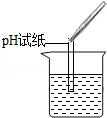 |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
分析 【学生板演】
氢氧化钠和稀硫酸反应生成硫酸钠和水;
【实验探究】
氢氧化钠能和硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠;
稀硫酸显酸性,pH小于7;
碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳;
钡离子和硫酸根离子能够结合成白色沉淀硫酸钡;
【实验探究】
测定溶液酸碱度的方法是:用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH;
【拓展延伸】
氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水;
碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
根据反应的化学方程式和提供的数据可以计算该氢氧化钠溶液的溶质质量分数.
解答 解:【学生板演】
氢氧化钠和稀硫酸反应生成硫酸钠和水,该反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O.
故填:2NaOH+H2SO4═Na2SO4+2H2O.
【假设猜想】
不合理的猜想是猜想四,不合理的理由是硫酸和氢氧化钠不能共存.
故填:猜想四;硫酸和氢氧化钠不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
故填:NaOH.
(2)实验过程如下表所示:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 产生气泡 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
| A.物质的分类 | B.用“化学”眼光分析 |
| ①玻璃、塑料都属于无机非金属材料 ②含碳的化合物都属于有机物 ③涤纶、羊毛和棉花属于天然纤维 | ①工业制汽水时,利用 加压的方法使大量的二氧化碳气体溶解在水里 ②地里庄稼出现叶色发黄需施用氮肥 ③装食品用的聚乙烯塑料袋可以通过加热进行封口 |
| C.“元素与健康”的关系 | D.物质的俗称、学名与化学式 |
| ①做菜时用铁强化酱油调味防治贫血 ②大米给人体提供的营养素是蛋白质 ③氟、铁、钠是人体所需的微量元素 | ①酒精 乙醇 C2H6O ②盐酸 氢氯酸 HCl ③铜绿 氢氧化铜 Cu2(OH)2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取11.6g纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式 Na2CO3+CaCl2═CaCO3↓+2NaCl |
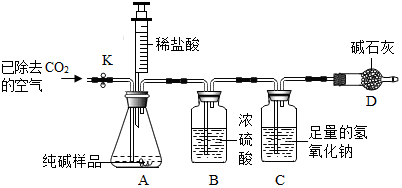
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量 的CaCl2溶液. | 有白色沉淀产生 | 该反应的方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②将上述反应后的混合液过滤,取滤液. | 有气泡冒出 | 证明猜想②成立. |
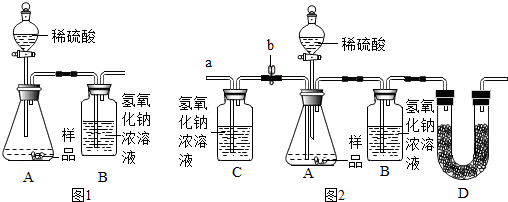
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com