
【题目】甲、乙二个实验用于验证水的性质。
甲:验证水与二氧化碳反应 | 乙:验证水与生石灰反应 |
|
|
①写出甲实验化学反应方程式_________。步骤二,胶头滴管中试剂名称是________。
②乙实验发生反应时出现现象是________。
③甲、乙实验都使用酸碱指示剂,其目的是______________。
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:
【题目】下面是部分原子或离子的结构示意图.请仔细观察、分析,再回答问题:
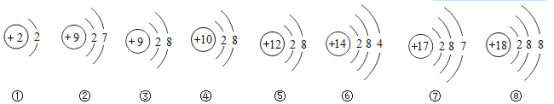
(1)上述粒子中属于阳离子的是_________________;(填序号),属于阴离子的是___________(填序号)。
(2)上述粒子中属于稳定结构的原子是_________________;(填序号).可见,元素的化学性质与原子的________________关系密切。
(3)写出⑤和⑦形成化合物的化学式______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
(1)高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比为_______(填最简比);
(2)现用447 kg次氯酸钠制得了800 kg含杂质的高铁酸钠粗产品,请问制得的产品中高铁酸钠的质量分数为多少_______?(要求写出具体的解答过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。下列说法错误的是( )
物质 | A | B | C | D |
反应前质量/g | 4 | 6 | 111 | 4 |
反应后质量/g | 待测 | 6 | 0 | 84 |
A.该闭容器中发生的化学变化属于分解反应
B.反应中B这种物质可能是催化剂
C.该反应中A、C、D四种物质(参加反应或生成)的质量比为35∶111∶80
D.反应后密闭容器中待测A的质量为35 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学学科特有的思维方式。
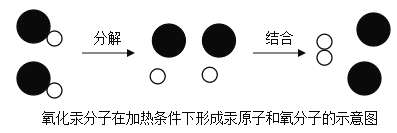
①保持氧化汞化学性质的微粒是____________(填化学式)。
②写出氧化汞加热反应的化学方程式___________,该反应的反应类型是_____________。
③对微粒示意图的理解错误的是________________。
A 每二个氧原子可以构成一个氧分子
B 原子可以直接构成物质
C 反应前后氧、汞元素存在形态都发生变化
D 反应过程中氧元素的化合价降低为 0 价
E 反应前后分子种类不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家成功研发出一种合成甲醇的新工艺,其反应过程的微观示意图如下。请回答下列问题:
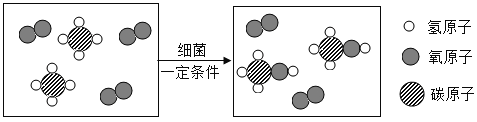
(1)图示中总共有________种分子。
(2)图示中属于单质的物质的化学式是_______;保持其化学性质的最小粒子是_______;
(3)写出图中相关反应的化学方程式:________;该反应的基本类型是_________;
(4)参加该反应的反应物的质量比是_______;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组为验证质量守恒定律,按照如图装置进行实验,称取24g镁粉在空气中燃烧,发现产物中有少量黄色固体。
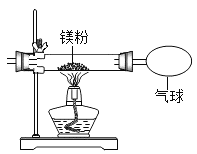
[提出问题]黄色固体是什么呢?
[查阅资料]①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
[做出猜想]黄色固体是Mg3N2。
[实验探究]请设计实验,验证猜想。
实验操作 | 实验现象及结论 |
取燃烧后的产物于试管中,加少量_________,再将______放在试管口,观察现象 | 观察到________,说明燃烧产物中含有Mg3N2 |
[反思与交流](1)Mg3N2中氮元素的化合价为________。
(2)空气中N2的含量远大于O2的含量,而镁粉在空气中燃烧生成的MgO却远多于Mg3N2,其原因是_______。
(3)写出镁粉在氮气中燃烧的化学方程式_______。
(4)镁粉还可以在CO2中燃烧,反应生成一种白色氧化物和一.种黑色固体,写出该反应的化学方程式:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了测定空气中氧气体积含量的实验:在试管内放入白磷,塞上胶塞,将试管放入热水中,使白磷燃烧;冷却后将试管倒立于盛水的水槽中,如图所示。
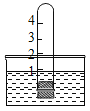
(1)取下胶塞后应观察到的现象是________;此装置的优点是:_________(任答一点即可):
(2)为确保实验成功,你认为在实验过程中应注意的问题(至少写两点)_______、_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:

(1)用图中序号表示配制溶液的正确操作顺序___________________;
(2)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaC1质量为____________________g。
(3) NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的质量分数________;(填“大于”、“小于”或“等于”) 10%。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com