

| 64(x+y) |
| 12.7g |
| 44x |
| 4.4g |
| 44x |
| 4.4g |
| 18(x+2y+z) |
| 7.2g |
| 1 |
| 4 |
| 1 |
| 4 |
| ||
| ||


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
| 碳酸钠 | 碳酸氢钠 | |
| 与盐酸反应 | Na2CO3+2HCl= |
NaHCO3+HCl= |
| 注意:不宜用上述反应制CO2的原因是 胃溃疡不宜选择NaHCO3缓解胃酸过多的原因是 | ||
| 与石灰水反应 | Na2CO3+Ca(OH)2= |
/ |
查看答案和解析>>
科目:初中化学 来源: 题型:
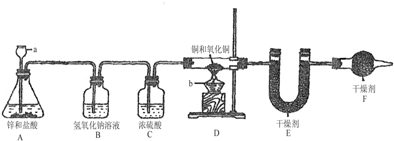
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | / | 9.8 | 480 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | 0.2g氧化铁 | 67 | 89.5 |
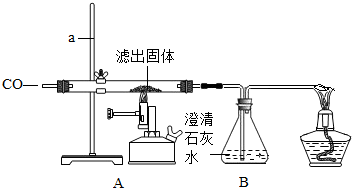
| 装置 | 现象 | 结论 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是甲、乙、丙三种物质的溶解度曲线.请回答:
如图是甲、乙、丙三种物质的溶解度曲线.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.当加入熟石灰mg时,溶液中的溶质为
用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.当加入熟石灰mg时,溶液中的溶质为查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、因为熟石灰能和酸发生反应,所以可用熟石灰改良酸性土壤 |
| B、因为“洗洁精”有乳化功能,所以“洗洁精”可用来洗涤餐具上的油污 |
| C、因为一氧化碳有还原性,所以可置换出铁的氧化物中的铁元素 |
| D、因为氮气化学性质不活泼,所以可用于食品包装袋内防腐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com