
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加人5g |
| 剩余固体的质量 | 3g | 2g | l g | 1g |
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
根据反应的化学方程式和表中提供的数据可以进行相关方面的判断和计算.
解答 解:设5g稀盐酸中氯化氢质量为x,
由表中数据可知,前3次中,5g稀盐酸恰好和1g碳酸钙反应,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73
1g x
$\frac{100}{1g}$=$\frac{73}{x}$,
x=0.73g,
该稀盐酸的溶质质量分数为:$\frac{0.73g}{5g}$×100%=14.6%,
答:该稀盐酸的溶质质量分数为14.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:选择题
| A. | 减少使用不必要的塑料品,可用纸袋代替塑料袋 | |
| B. | 减少分类回收各种废弃塑料的程序 | |
| C. | 使用一些新型的、可降解的塑料 | |
| D. | 在家重复使用塑料袋 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 锌 | B. | 镁 | C. | 铜 | D. | 铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
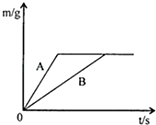 将等质量的锌粉和铁粉(颗粒大小相同),分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.
将等质量的锌粉和铁粉(颗粒大小相同),分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某固体混合物A中可能含硫酸钠、碳酸钠、硝酸钡、氯化铵等物质中的若干种.按如图所示进行实验,出现的现象如图所述(实验过程中所有发生的反应都恰好完全反应).
某固体混合物A中可能含硫酸钠、碳酸钠、硝酸钡、氯化铵等物质中的若干种.按如图所示进行实验,出现的现象如图所述(实验过程中所有发生的反应都恰好完全反应).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在汽油中加入适量的乙醇可以一定程度减少汽车尾气的污染 | |
| B. | 因制取成本高和贮存困难,氢气作为燃料和化学电源暂时还未能应用 | |
| C. | 金属的回收利用,既可以节约金属资源又可以节约能源,还可以减少对环境的污染 | |
| D. | 空气的成分按体积计大约是:氧气21%、氮气78%、稀有气体等其他成分1% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com