
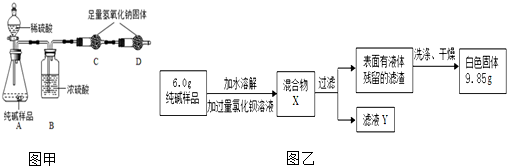
分析 【实验步骤】①根据实验制取气体首先要装置的气密性进行解答;
【实验分析】(1)根据碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳进行解答;
(2)根据浓硫酸具有吸水性进行解答;
(3)根据C装置中增加的质量就是生成的二氧化碳的质量,如果没有B装置,会使测得生成二氧化碳的质量增大进行解答;
(4)根据盐酸挥发出氯化氢气体被装置C吸收,影响实验测定进行解答;
(5)根据C装置前后质量增加的质量就是生成的二氧化碳的质量进行解答;
(二)(1)根据氯化钡溶液和碳酸钠反应生成碳酸钡沉淀进行解答;
(2)根据氯化钠和硝酸银溶液反应生成氯化银白色沉淀进行解答;
(3)根据白色固体就是生成的碳酸钡的质量求出碳酸钠的质量即可;
【实验反思】根据因甲组中生成的二氧化碳残留在锥形瓶中,未被装置C吸收,影响实验测定进行解答.
解答 解:【实验步骤】①根据实验制取气体首先要装置的气密性;
【实验分析】(1)碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,A装置中反应的化学方程式为Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
(2)浓硫酸具有吸水性,所以B装置的作用是除去水蒸气;
(3)C装置中增加的质量就是生成的二氧化碳的质量,如果没有B装置,会使测得生成二氧化碳的质量增大,所以碳酸钠的质量也增多,故没有B装置则所测样品中碳酸钠的质量分数偏大;
(4)盐酸挥发出氯化氢气体被装置C吸收,影响实验测定,所以不能用盐酸代替硫酸;
(5)设样品中碳酸钠的质量为x.
二氧化碳的质量=65.6g-61.2g=4.4g
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
样品中碳酸钠的质量分数=$\frac{10.6g}{13.0g}×100%$=81.5%
答:样品中碳酸钠的质量分数为81.5%.
(二)(1)氯化钡溶液和碳酸钠反应生成碳酸钡沉淀,所以判断加入氯化钡溶液是否过量的合适方法是静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量;
(2)氯化钠和硝酸银溶液反应生成氯化银白色沉淀,所以判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加硝酸银溶液;
(3)设原混合物中碳酸钠的质量是y
Na2CO3+BaCl2=BaCO3↓+2NaCl
106 197
y 9.85g
$\frac{106}{y}=\frac{197}{9.85g}$
y=5.3g
乙组测得样品中碳酸钠的质量分数=$\frac{5.3g}{6.0g}×100%$=88.3%
答:乙组测得样品中碳酸钠的质量分数为88.3%.
白色固体就是生成的碳酸钡的质量求出碳酸钠的质量即可;
【实验反思】根据因甲组中生成的二氧化碳残留在锥形瓶中,未被装置C吸收,影响实验测定,所以甲乙两组同学所测该品牌中碳酸钠的质量分数,乙组更准确.
故答案为:
【实验步骤】①装置的气密性;
【实验分析】(1)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;(2)除去水蒸气;(3)偏大;
(4)盐酸挥发出氯化氢气体被装置C吸收,影响实验测定;(5)81.5;
(二)(1)A;(2)C;(3)88.3;
【实验反思】乙;因甲组中生成的二氧化碳残留在锥形瓶中,未被装置C吸收,影响实验测定.
点评 此题是一道实验探究综合题,充分的展示了化学知识的方方面面,该题综合性强难度较大,对训练学生良好地思维品质以及知识的严密性有较好的帮助.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | NaOH→Na2SO4 | B. | CuO→Cu(OH)2 | C. | CuCl2→Cu | D. | BaCl2→BaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2:3 | B. | 3:2 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
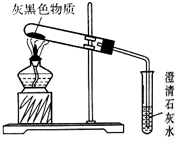 镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为是MgO;乙同学认为是Mg2(OH)2CO3;丙同学认为是Mg(OH)2.
镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为是MgO;乙同学认为是Mg2(OH)2CO3;丙同学认为是Mg(OH)2.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
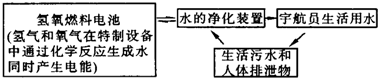
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
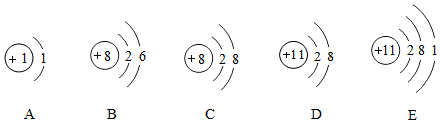
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com