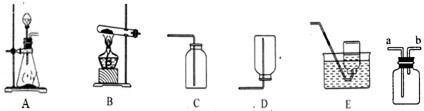
解:(1)制取氨气如同制取氧气:使用固体+固体反应,需加热,所以选用B装置;
(2)演示高锰酸钾粉末加入试管中的操作方法;
(3)制取气体的注意事项,检查装置的气密性方法;
(4)实验室利用过氧化氢溶液和二氧化锰混合制O
2应选择制取装置,选用B装置,为防反应速率过快,应提出的实验安全注意事项:控制液体的滴加速率.
(5)①过氧化氢制取氧气的反应装置和反应原理:固体+液体,且不需要加热,所以选用 A装置 2H
2O
2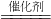
2H
2O+O
2↑;了解注意事项;②比较制取氧气的两种装置的区别:是否需要加热;
(6)用排水法收集的氧气中混入了空气:①集气瓶没有装满水,有气泡或②没有等到气泡均匀快速连续的冒出,便开始收集;
(7)氨气的密度小于空气,所以用向下排空气法;加热氯化铵和氢氧化钙的固体混合物制取氨气:它又极易溶于水,反应条件就决定了制取氨气必须在干燥的环境下,加之密度比空气小.
故答为:(1)B E 高锰酸钾

锰酸钾+二氧化锰+氧气 防止加热有水生产,水倒流,引起试管炸裂
(2)试管横放,用纸槽或药匙将高锰酸钾粉末加入试管底部
(3)装置气密性差
(4)把导管伸入水槽 用双手捂住瓶子 有气泡冒出
(5)A 过氧化氢
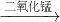
水+氧气 过氧化氢溶液 ①不需要加热,反应条件简单
(6)集气瓶没有装满水,有气泡
(7)B D
分析:(1)高锰酸钾制取氧气的反应装置和反应原理:固体+固体,且需要加热,所以选用B装置,了解注意事项;
(2)将粉末加入试管中的操作方法;
(3)检查装置的气密性方法,进行简单操作;
(4)氧气、二氧化碳、氨气的收集和检验方法比较.
(5)①过氧化氢制取氧气的反应装置和反应原理:固体+液体,且不需要加热,所以选用 A装置 2H
2O
2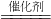
2H
2O+O
2↑;了解注意事项;②比较制取氧气的两种装置的区别:是否需要加热;
(6)用排水法收集的氧气中混入了空气:①集气瓶没有装满水,有气泡或②没有等到气泡均匀快速连续的冒出,便开始收集;
(7)加热氯化铵和氢氧化钙的固体混合物制取氨气:氨气又极易溶于水,反应条件就决定了制取氨气必须在干燥的环境下,加之密度比空气小所以可以采用向上排空气法收集.
点评:(1)此题重在考查同学们对常用化学仪器的了解和识记情况,只有很好的认识它们,做试验才能得心应手.
(2)重在考查氧气的实验室制法,加热高锰酸钾可以得到氧气,分解过氧化氢也可以得到氧气,但是各自的实验条件不同,一定注意区分;与二氧化碳的制取比较.
(3)属于扩展性问题,重在考查根据物质的物理和化学性质制备物质,题中采用氨气只是为了举例分析.


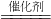 2H2O+O2↑;了解注意事项;②比较制取氧气的两种装置的区别:是否需要加热;
2H2O+O2↑;了解注意事项;②比较制取氧气的两种装置的区别:是否需要加热; 锰酸钾+二氧化锰+氧气 防止加热有水生产,水倒流,引起试管炸裂
锰酸钾+二氧化锰+氧气 防止加热有水生产,水倒流,引起试管炸裂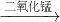 水+氧气 过氧化氢溶液 ①不需要加热,反应条件简单
水+氧气 过氧化氢溶液 ①不需要加热,反应条件简单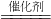 2H2O+O2↑;了解注意事项;②比较制取氧气的两种装置的区别:是否需要加热;
2H2O+O2↑;了解注意事项;②比较制取氧气的两种装置的区别:是否需要加热;

 科学实验活动册系列答案
科学实验活动册系列答案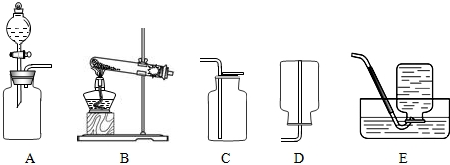

 35、下列是实验室常用仪器示意图.
35、下列是实验室常用仪器示意图. 27、下列是实验室常用仪器的示意图.
27、下列是实验室常用仪器的示意图.