
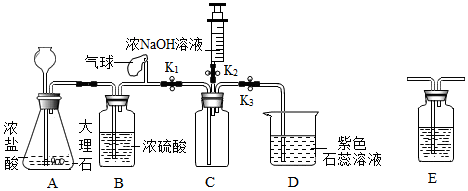
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳溶于水生成碳酸,碳酸能使紫色石蕊试液变红进行解答;
(2)根据二氧化碳中常含有氯化氢气体和水蒸气,所以应该先用洗气瓶E除去氯化氢进行解答;
(3)根据二氧化碳和NaOH溶液反应生成碳酸钠和水,C内压强减小进行解答;
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,二氧化碳溶于水生成碳酸,碳酸能使紫色石蕊试液变红,所以当观察到装置D中的现象是紫色石蕊试液变红.可确定装置C收集满CO2;
(2)二氧化碳中常含有氯化氢气体和水蒸气,所以应该先用饱和NaHCO3溶液除去氯化氢,所以应该在A、B之间加入洗气瓶E;
(3)二氧化碳和NaOH溶液反应生成碳酸钠和水,C内压强减小,所以实验方案是:将注射器中的5mL水压入到装置C中,重复实验,观察到液体倒吸的量小于推入NaOH实验时的量,说明CO2与NaOH发生反应.
故答案为:(1)CaCO3+2HCl=CaCl2+CO2↑+H2O,变红;
(2)A和B,除去二氧化碳中的氯化氢气体;
(3)水.
点评 本题以实验探究的形式考查氢氧化钠、二氧化碳的性质,同学们要具有综合的化学知识才能做好此题.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:选择题
| A. | H2、O2、CO | B. | H2、O2、CO2 | C. | HCl、SO2、CO2 | D. | O2、SO2、SO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
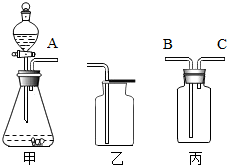 如图是实验室常用装置.
如图是实验室常用装置.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
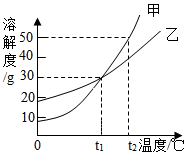 甲、乙两种物质的溶解度曲线如图所示.下列说法不正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲和乙的饱和溶液从t1℃升温到t1℃时都有晶体析出 | |
| C. | t1℃时,甲和乙的饱和溶液各100g其溶质的质量相等 | |
| D. | t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com