
分析 (1)根据质量守恒定律计算反应后生成的二氧化碳的质量;
(2)根据二氧化碳的质量结合化学方程式计算碳酸钠的质量,再计算质量分数;
解答 解:(1)根据质量守恒定律可知,生成的为:6g+61.7g-65.5g=2.2g;
(2)设6g纯碱样品中含碳酸钠的质量为x.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
所以该样品中纯碱的质量分数=$\frac{5.3g}{6g}$×100%=88.3%;
答:产生二氧化碳为2.2g,样品中含纯碱的质量分数为88.3%.
点评 本题主要考查根据化学方程式的计算,难度不大,需要首先搞清反应原理,然后结合题中所给的数据进行解答.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水结冰后,质量保持不変 | |
| B. | 铜粉在空气中加热后,质量增大 | |
| C. | 8g氢气在8g氧气中点燃完全反应后,生成9g水 | |
| D. | 1.2g碳与3.2g氧气完全反应,生成4.4g二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | CuO(C) | 在空气中充分灼烧 |
| B | H2O(H2O2) | 加入少量二氧化锰,充分反应后,过滤 |
| C | CaO(CaCO3) | 高温煅烧 |
| D | CO(CO2) | 将混合气体依次通过灼热的氧化铜和澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
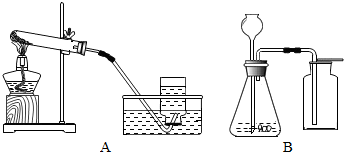 如图是初中化学实验中常用的两套装置,请依据题目要求回答有关问题:
如图是初中化学实验中常用的两套装置,请依据题目要求回答有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com