
【题目】在一定条件下,氨气容易液化而成为液氨。液氨可以燃烧,其燃烧的化学方程式为
4NH3+3O2 ![]() 2X+6H2O。下列说法中正确的是( )
2X+6H2O。下列说法中正确的是( )
A. 液氨属于混合物 B. NH3中N元素的化合价为–1价
C. X的化学式为NO D. 液氨具有可燃性,可用作燃料
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下列做法,能达到实验目的是![]()
A. 用铁丝代替红磷,粗略地测定空气中氧气的含量
B. 用25mL蒸馏水和25mL酒精配制50mL酒精溶液
C. 将气体通入足量氢氧化钠溶液,除去![]() 中少量的CO
中少量的CO
D. 将稀硫酸滴在金属表面,鉴别真黄金和假黄金![]() 铜锌合金
铜锌合金![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年3月,国务院总理李克强在政府工作报告中强调:“坚决打好蓝天保卫战”山西省积极行动,落实整改措施,省城太原首先通过以下三种方式缓解空气污染初见成效。



A.电动出租车 B.垃圾清扫车 C.喷水雾汽车
(1)为了使空气更新,天空更蓝,你作为环保小卫士,认为推广使用上述方式的好处是 (任选一项回答)
(2)空气污染严重损害人体健康,影响作物生长,破坏生态平衡引起空气污染的有害气体种类很多,请举一例 (用化学式表示)
(3)你认为改善空气质量的措施正确的是
a.推广使用新能源
b.加强企业排污管理
c.雾霾多发天气,实行私家车限号出行。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾与氯化钾的溶解度曲线如图所示,请回答下列问题。
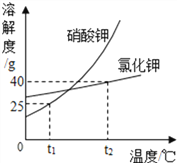
(1)t1℃时,两物质中溶解度较大的是________;
(2)t2℃时,两物质的等质量饱和溶液降温至t1℃,过滤,所得硝酸钾溶液质量__________所得氯化钾溶液质量;(填“>”、“=”或“<”)
(3)t2 ℃时,将100g水加人盛有50g氯化钾的烧杯中,充分溶解后,得到溶液质量为_______g;
(4)欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们知道铁的化学性质比较活泼,能与氧气、酸、CuSO4溶液等多种物质发生化学反应。化学兴趣小组在课外资料中发现,铁和Fe2O3竟然也能发生化学反应。
【提出问题】
铁和Fe2O3反应的产物是什么?
【查阅资料】
①FeO、Fe2O3、Fe3O4中,Fe2O3是红棕色,其余是黑色;FeO在空气中会很快被氧化成Fe2O3;Fe3O4有磁性。②二氧化碳可用作该反应的保护气。③铁的氧化物都能与酸溶液反应。
【猜想与假设】
根据质量守恒定律,请你猜想铁和Fe2O3反应的产物:
①有FeO;②只有Fe3O4;③ 。
【进行实验】
(1)按下图装好药品(铁粉过量),连好仪器(装入药品前已检查装里的气密性)。
(2)轻推注射器活塞通入二氧化碳,估计玻璃管里空气 ,停止通入二氧化碳。
(3)点燃酒精喷灯加热药品,等到固体粉末全部变黑,再熄灭酒精喷灯。
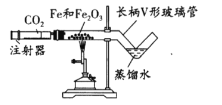
(4)当长柄V形玻璃管冷却至室温时,检验黑色粉末成分。检验过程如下(请填写表格中的空白):

【探究结论】
铁和Fe2O3能发生化合反应,有关的化学方程式是 。
【反思评价】
(1)实验结束,微热V形管中的液体,发生反应的化学方程式是 。
(2)本实验中的保护气,既能用二氧化碳气体,也能用 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映其对应变化关系的是( )
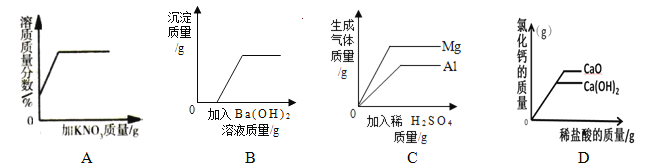
A. 一定温度下,向不饱和KNO3溶液中加入KNO3固体
B. 向硝酸和硫酸铜的混合溶液中滴加氢氧化钡溶液
C. 向等质量的金属镁和铝中分别加入等质量且质量分数相等的足量稀硫酸
D. 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示-——表示物质两两之间能发生化学反应。请根据如图,回答问题。(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)


(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈_________________(填“酸性、碱性或中性”)。
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是________________,此时含有的溶质有________(酸碱指示剂除外)(用化学式填空,下同)。
(3)为验证乙同学所得溶液中含有的溶质,可取少量反应后的溶液滴加过量的____________溶液(填一种物质的化学式),产生_______________________________现象,则证明存在。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有100g废液,其中含有硫酸铜、硫酸亚铁、硫酸锌。现对废液进行处理,得到铜和硫酸锌溶液,实验流程如下图所示。
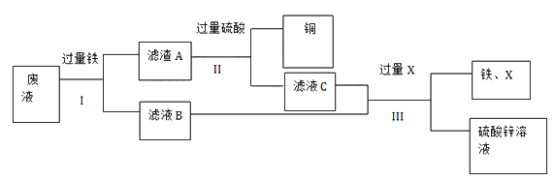
(1)步骤I、II、III中均包含的操作名称是____。
(2)滤液B中的溶质是____________________。(填化学式)
(3)当观察到_________时,说明滤渣A中铁已经完全反应。
(4)步骤III中加入的X是________。 (填化学式)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁、铝、铜是常见的三种金属.同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
操作 |
|
|
| 根据现象得出金属活动性顺序 |
片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 | |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面的氧化物会先与盐酸反应.
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是 .
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出金属活动性顺序 |
现象 | 无明显现象 | | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式 .
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为 .
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com