

分析 【猜测】根据碳的氧化物可能是一氧化碳,也可能是二氧化碳,也可能是一氧化碳和二氧化碳进行分析;
【实验探究】①根据二氧化碳能使澄清石灰水变浑浊进行分析;
②根据加热条件下,氧化铜能和一氧化碳反应生成铜和二氧化碳进行分析;
【实验结论】根据草酸在加热的条件下生成二氧化碳、一氧化碳和水进行分析;
【问题讨论】①根据氢氧化钠能够吸收二氧化碳,浓硫酸有吸水性进行分析;
②根据一氧化碳有毒,需要尾气处理进行分析.
解答 解:【猜测】碳的氧化物可能是一氧化碳,也可能是二氧化碳,也可能是一氧化碳和二氧化碳,所以
猜想1:只有CO;
猜想2:只有CO2;
猜想3:含有CO和CO2;
【实验探究】①二氧化碳能使澄清石灰水变浑浊,所以观察到A装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成;
②有两种实验现象都能分别证明草酸分解的气体中含有CO,分别是:
C中石灰水不变浑浊,F中澄清石灰水变浑浊;
E装置中出现:黑色粉末变成红色粉末;
【实验结论】草酸在加热的条件下生成二氧化碳、一氧化碳和水,化学方程式为:C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O;
【问题讨论】①氢氧化钠能够吸收二氧化碳,浓硫酸有吸水性,所以B装置的作用是吸收二氧化碳,D装置的作用是吸收水分;
②一氧化碳有毒,需要尾气处理,所以装置末端酒精灯的作用是处理尾气CO;
故答案为:猜想2:CO2;
(1)A;
(2)①F中澄清石灰水变浑浊;
②黑色氧化铜变成红色物质;
【实验结论】H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+H2O;
【问题讨论】点燃尾气中一氧化碳,防止污染空气.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | 用稀硫酸除铁锈 | |
| B. | 施用熟石灰改良酸性土壤 | |
| C. | 用氢氧化钠溶液洗涤石油产品中残余的硫酸 | |
| D. | 服用含氢氧化铝的药物(如斯达舒)来治疗胃酸过多 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
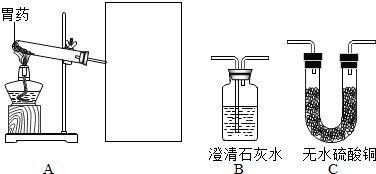
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
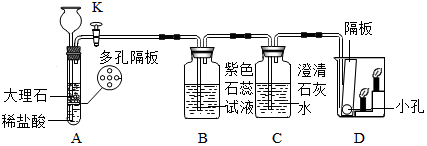
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 归纳是学习化学的重要方法.小明总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:
归纳是学习化学的重要方法.小明总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
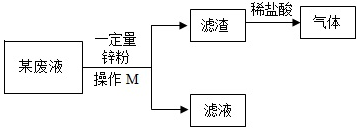
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中. | 木条不复燃 | 常温下过氧化氢溶液分解很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 加入水泥块能加快过氧化氢溶液的分解速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com