
分析 (1)根据钙元素的生理功能进行分析.
(2)根据灭火的方法考虑;
(3)根据生石灰与水的反应写出反应的化学方程式;
(4)根据洗涤剂洗油污的原理考虑;
(5)日常生活中可采用煮沸的方法将硬水软化.
(6)有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物,据此常见材料的分类进行分析判断.
(7)根据铁生锈的条件分析回答.
(8)维生素C高温易分解;食醋与碱能发生中和反应;进行分析.
(9)溶质的质量=溶液的质量×溶质的质量分数,
(10)书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.
解答 解:(1)青少年处于生长发育期,为预防患佝偻病,可以多吃奶制品、虾皮等食物,补充人体需要的钙元素.故填:钙;
(2)森林火灾时,常砍伐出一条隔离带的目的是隔离可燃物;故填:隔离可燃物;
(3)某饼干包装袋中用生石灰作干燥剂,是由于生石灰能与水化合生成了氢氧化钙,反应的化学方程式是:CaO+H2O═Ca(OH)2;故填:CaO+H2O═Ca(OH)2;
(4)洗涤剂清洗餐具上的油污是将油污分解成小的油滴,被水冲走,利用了乳化原理,所以说明洗涤剂具有乳化的功能;故填:乳化;
(5)日常生活中可采用煮沸的方法将硬水软化;故填:煮沸.
(6)A、不锈钢炊具是用不锈钢制成的,属于金属材料.
B、橡胶手套是用合成橡胶制成的,合成橡胶属于三大合成材料之一.
C、纯棉围裙是用羊毛制成的,纯棉属于天然材料.
故填:B;
(7)对铁质栅栏进行喷漆处理可以防止其生锈,原因是隔绝空气和水.故填:喷漆;
(8)维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,证明其显酸性;加热该溶液至沸腾,红色消失,说明维生素C高温易分解;因此烹调时不要高温加热.食醋与碱能发生中和反应,烧煮时能减少维生素C的消耗;因此烧煮时能起到保护维生素C的作用.故填:酸;不要高温加热;食醋;
(9)要配制150kg16%的氯化钠溶液,需要氯化钠150kg×16%=24kg;溶液中存在的阳离子是钠离子;故填:24;Na+;
(10)硝酸铵受撞击时易分解产生一氧化二氮气体和无色液体--水.该反应的化学方程式为:NH4NO3$\frac{\underline{\;撞击\;}}{\;}$N2O↑+2H2O;故填:NH4NO3$\frac{\underline{\;撞击\;}}{\;}$N2O↑+2H2O.
点评 本题难度不大,掌握物质的性质、灭火原理、质量守恒定律等是解答本题的关键.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 有机物中都含有碳元素,所以含碳元索的物质都是有机物 | |
| B. | 酸雨的PH小于7,所以pH小于7的雨水一定是酸雨 | |
| C. | 各种酸溶液中都含有氢离子(H+),因此酸溶液具有许多相似的化学性质 | |
| D. | 碳酸盐能与稀盐酸反应放出气体,则与稀盐酸反应放出气体的物质一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
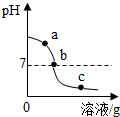 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小明和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小明和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | 只产生白色沉淀(产生白色沉淀也可) | 该样品为b处溶液. |
| 先产生气泡,后产生白色沉淀 | 该样品为c处溶液. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 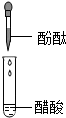 检验醋酸是否有酸性 | B. | 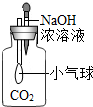 小气球变瘪 | ||
| C. | 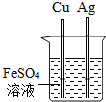 验证Fe、Cu、Ag的金属活泼性强弱 | D. | 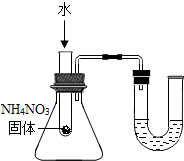 U型管内液面左高右低 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸与碱发生中和反应时有热量放出,所以有热量放出的反应一定是中和反应 | |
| B. | 酸雨的pH小于7,因此pH小于7的雨水一定是酸雨 | |
| C. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| D. | 合金是在某种金属中加热熔合其他金属或非金属形成的,所有合金一定属于混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com