

分析 (1)铁和铜都属于金属材料,塑料属于有机高分子材料;
(2)铁在有水和空气并存的条件下易生锈;
(3)
①一氧化碳能够还原氧化铁生成二氧化碳和铁,据此结合化学方程式的书写规则回答问题即可;
②在金属活动性顺序中,铁和铜排在银的前面,可以将硝酸银中的银置换出来.
解答 解:
(1)根据图示给出的材料可知,铸铁管是由铁的合金制成和铜管属于金属单质,两者都属于金属材料,塑料管则属于有机高分子材料;
(2)因为铁在有水和氧气并存的条件下易生锈;
(3)①一氧化碳还原氧化铁会生成铁和二氧化碳,其方程是为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②在金属活动性顺序中,铁和铜排在银的前面,可以将硝酸银中的银置换出来,所以剩余固体中肯定含银,铁和铜的量不确定,故不能确定是否含铁和铜.分析选项AC正确;
答案:
(1)A、B;
(2)水与氧气并存;
(3)
①3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②AC
点评 本题考查了常见金属的性质,完成此题,可以依据已有的知识结合题干提供的信息进行.


科目:初中化学 来源: 题型:选择题
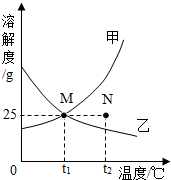 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | 在t1℃时,甲、乙两物质的溶解度相等 | |
| C. | 在t2℃时,N点表示甲物质的不饱和溶液 | |
| D. | 在t1℃时,甲物质的饱和溶液中溶质的质量分数是25% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
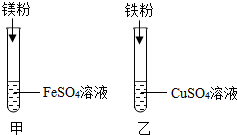 化学小组同学设计了如图所示实验方案.
化学小组同学设计了如图所示实验方案.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 性质 | 用途 |
| 干冰 | 升华吸热 | ①做制冷剂 |
| 生石灰 | ②与水反应生成氢氧化钙 | 用作干燥剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
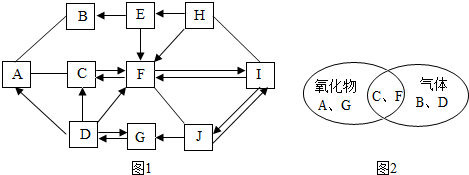
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16g | B. | 8g | C. | 5.6g | D. | 无法计算 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
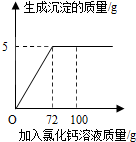 向50gNa2CO3溶液中逐滴加入一定溶质质量分数的CaCl2溶液.实验过程中,生成沉淀质量与加入CaCl2溶液的质量关系如图所示,试计算:
向50gNa2CO3溶液中逐滴加入一定溶质质量分数的CaCl2溶液.实验过程中,生成沉淀质量与加入CaCl2溶液的质量关系如图所示,试计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com