
| A、铁 | B、锌 | C、铝 | D、铜 |
| x |
| 24g |
| 2 |
| 2.1g |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:
| A、HCl、Ca(OH)2、KNO3 |
| B、NaCl、NaNO3、CuSO4 |
| C、HCl、BaCl2、H2SO4 |
| D、K2CO3、NaOH、HNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
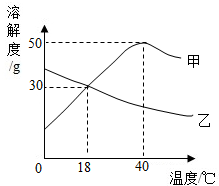 甲、乙两种固体物质的溶解度曲线如图所示,根据图中的信息判断,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,根据图中的信息判断,下列说法正确的是( )| A、甲的溶解度大于乙的溶解度 |
| B、降低温度可使甲、乙的饱和溶液变为不饱和溶液 |
| C、18℃时,甲、乙两种过饱和溶液的溶质质量分数相等 |
| D、物质甲的溶解度随温度的升高而升高 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 物质 | 杂质 | 试剂 |
| A | CuO | C | 足量空气 |
| B | CO2 | HCl | 足量氢氧化钠溶液和浓硫酸 |
| C | KCl | K2SO4 | 蒸馏水和过量BaCl2溶液 |
| D | FeCl3溶液 | CuCl2 | 过量铁粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:
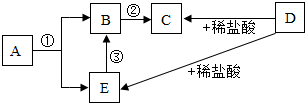 A、B、C、D、E、F均为初中常见的物质,它们之间的关系如图所示.(“→”表示转化关系,部分生成物及反应条件已略去).
A、B、C、D、E、F均为初中常见的物质,它们之间的关系如图所示.(“→”表示转化关系,部分生成物及反应条件已略去).查看答案和解析>>
科目:初中化学 来源: 题型:
| A、16:11 | B、16:9 |
| C、9:11 | D、4:9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com