【答案】
分析:(1)根据实验常用仪器回答;
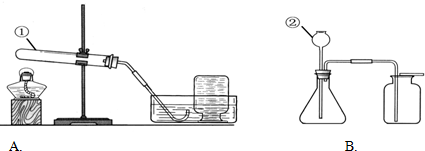
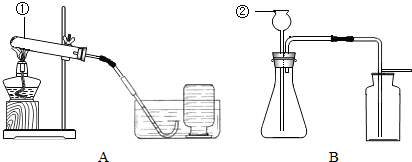
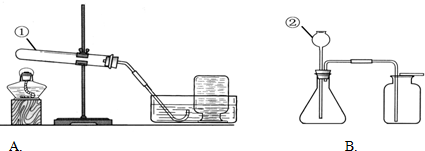
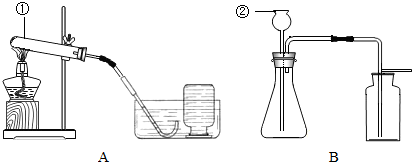
(2)①A装置是用加热固体的方法制取氧气,且试管口无棉花,所以是利用氯酸钾制取氧气,然后依据氯酸钾分解反应原理书写方程式;
②用排水法集气时,说明氧气已收集满的现象是:瓶口有气泡冒出;氧气的密度比空气大,所以应正放在桌面上;
(3)①分析B装置特点,确定用此装置制取氧气的药品,再依据反应原理书写方程式;
②依据大理石与稀盐酸反应原理书写方程式,证明二氧化碳是否收集满的方法是:将燃着的木条放在集气瓶口,观察木条燃烧状况进行判断.
解答:解:
(1)根据实验常用仪器可知:仪器①是试管,②是长颈漏斗;
(2)①A装置是用加热固体的方法制取氧气,且试管口无棉花,所以是利用氯酸钾制取氧气; 氯酸钾在加热的条件下,二氧化锰作催化剂分解生成氯化钾和氧气,方程式是2KClO
3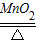
2KCl+3O
2↑;
②用排水法集气时,说明氧气已收集满的现象是:瓶口有气泡冒出;氧气的密度比空气大,所以应正放在桌面上;
(3)①B装置适用于固体和液体反应,且不需加热制取气体,过氧化氢分解制取氧气符合此条件,方程式是2H
2O
2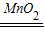
2H
2O+O
2↑;
②大理石与稀盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;证明二氧化碳是否收集满的方法是:将燃着的木条放在集气瓶口,观察木条燃烧状况进行判断,若熄灭,则收集满了;
故答案为:(1)①试管; ②长颈漏斗;(2)①2KClO
3
2KCl+3O
2↑; ②有气泡从集气瓶口冒出;向上;
(3)①2H
2O
2
2H
2O+O
2↑; ②CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;将燃着的木条放在集气瓶口,若木条熄灭,则二氧化碳已收集满.
点评:本题重点对实验室制取氧气和二氧化碳的反应方程式进行了考查,同时考查了氧气和二氧化碳的验满等知识,要掌握相关知识才能正确解答.


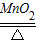 2KCl+3O2↑;
2KCl+3O2↑;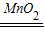 2H2O+O2↑;
2H2O+O2↑; 2KCl+3O2↑; ②有气泡从集气瓶口冒出;向上;
2KCl+3O2↑; ②有气泡从集气瓶口冒出;向上; 2H2O+O2↑; ②CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在集气瓶口,若木条熄灭,则二氧化碳已收集满.
2H2O+O2↑; ②CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在集气瓶口,若木条熄灭,则二氧化碳已收集满.

 口算能手系列答案
口算能手系列答案