
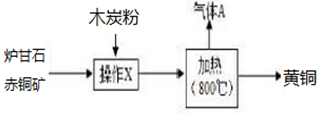
| A. | 操作X的名称是溶解 | |
| B. | 气体A一定为为纯净物 | |
| C. | 向黄铜中加入稀盐酸,会产生气泡 | |
| D. | 加热过程中一定有元素的化合价发生了改变 |
分析 A、反应物接触面积越大,反应速率越快;
B、木炭和氧化物反应时,生成的气体可能是二氧化碳,也可能是一氧化碳,也可能是二氧化碳和一氧化碳的混合物;
C、黄铜中含有锌和铜,其中的铜不能和稀盐酸反应,锌能和稀盐酸反应生成氯化锌和氢气;
D、化合物中元素的化合价代数和为零,单质中元素化合价规定为零.
解答 解:A、反应物接触面积越大,反应速率越快,因此操作X的名称是混合研磨,该选项说法不正确;
B、木炭和氧化物反应时,生成的气体可能是二氧化碳,也可能是一氧化碳,也可能是二氧化碳和一氧化碳的混合物,该选项说法不正确;
C、黄铜中含有锌和铜,其中的铜不能和稀盐酸反应,锌能和稀盐酸反应生成氯化锌和氢气,因此向黄铜中加入稀盐酸,会产生气泡,该选项说法正确;
D、反应前锌元素和铜元素存在于化合物中,化合价不能为零,反应后形成单质,化合价都为零,因此加热过程中一定有元素的化合价发生了改变,该选项说法正确.
故选:CD.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①③ | C. | ①④ | D. | ①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸碱中和反应生成盐和水,实验生成盐和水的反应一定是中和反应 | |
| B. | 酸性溶液的pH小于7,食醋是酸性溶液,所以食醋的pH小于7 | |
| C. | 原子在化学变化中不能再分,则分子在化学变化中也不能再分 | |
| D. | 水能灭火,所以电脑一旦失火应立即用水浇灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
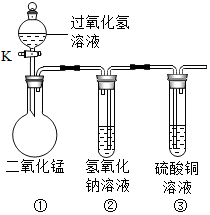 在“创新实验装置”的竞赛中,某化学兴趣小组的同学设计了如图所示的装置.
在“创新实验装置”的竞赛中,某化学兴趣小组的同学设计了如图所示的装置.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳、一氧化碳和二氧化碳都能还原氧化铜 | |
| B. | 一氧化碳、二氧化碳均为大气污染物 | |
| C. | 二氧化碳能使干燥的石蕊纸花变红 | |
| D. | 二氧化碳灭火同时利用了它的物理性质和化学性质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com