
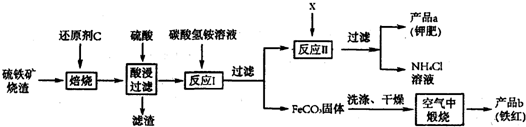
硫铁矿烧渣(主要成分是Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,下图为利用硫铁矿烧渣制备铁红(氧化铁)等产品的部分流程:

(1)写出流程中焦炭与Fe3O4反应的化学方程式_______________________________;
(2)酸浸、过滤后进入反应Ⅰ中的溶质主要是_______________;反应Ⅰ的温度一般需控制在35℃以下,其目的是_______________________________________________;
(3)将FeCO3固体洗涤、干燥的目的是_____________________________________;
(4)产品a的主要成分是K2SO4,检验产品a中是否含有氯化物(Cl-)的实验操作是:取少量产品a加适量的水溶解,__________________________。
(1) 2C+Fe3O4 3Fe+2CO2↑;
3Fe+2CO2↑;
(2)FeSO4(或FeSO4和H2SO4) ,防止NH4HCO3受热分解 ;
(3)除去表面的可溶性杂质,以得到纯净干燥的FeCO3,从而提高产品质量 ;
(4)加足量Ba(NO3)2溶液充分反应后过滤,往滤液中滴加AgNO3溶液观察有无沉淀
【解析】
试题分析:(1)焦炭具有还原性,在高温下能与Fe3O4反应,生成铁和二氧化碳,故反应的化学方程式为2C+Fe3O4 3Fe+2CO2↑;
3Fe+2CO2↑;
(2)因为Fe2O3、Fe3O4、FeO都与还原剂焦炭反应生成铁,而铁和稀硫酸反应,会生成硫酸亚铁和氢气,所以滤液中的主要溶质是硫酸亚铁;由于反应Ⅰ中加入了NH4HCO3溶液,而NH4HCO3受热易分解,故反应Ⅰ的温度一般需控制在35℃以下,以防止NH4HCO3受热分解;
(3)根据题意,煅烧FeCO3固体,能与氧气反应生成了氧化铁和二氧化碳,故为了提高产品质量,要将FeCO3固体洗涤、干燥,以便能得到纯净干燥的FeCO3;
(4)检验产品a中是否含有氯化物(Cl-),需要先除去SO42-,再来检验Cl-,所以要先滴加过量的Ba(NO3)2溶液,充分反应后过滤,过滤后再向滤液滴加AgNO3溶液,观察有无沉淀生成。
考点:物质分离和提纯的方法和基本操作综合应用,书写化学方程式
点评:解答本题时要掌握化学方程式的书写方法和实验方面的知识,只有这样才能对问题做出正确的判断。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com