
分析 (1)①根据工业制硫酸的流程为:FeS2→SO2$\stackrel{{O}_{2}}{→}$SO3$\stackrel{{H}_{2}O}{→}$H2SO4,因为其中有二氧化硫气体生成,则可推测工业制H2SO4可能会引起的环境问题.
②考虑在实验室中事故的紧急处理方法.
(2)考虑中和反应,利用化学方程式进行计算.
解答 解:(1)①根据工业制硫酸的流程为:FeS2→SO2$\stackrel{{O}_{2}}{→}$SO3$\stackrel{{H}_{2}O}{→}$H2SO4,因为其中有二氧化硫气体生成,则可推测工业制H2SO4可能会引起的环境问题为形成酸雨(或造成空气污染);
②因为浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的,而碳酸氢钠溶液显碱性,故在实验室中不慎将浓硫酸沾到皮肤上的紧急处理方法为立即用大量水冲洗,然后再涂上3%-5%的碳酸氢钠溶液中和残余硫酸.氢氧化钠和硫酸反应,反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O;
(2)沉淀不再产生,说明恰好中和,则此时液体的pH=7.
设化工产品中残留Ba(OH)2的质量为x.
Ba(OH)2+H2SO4═BaSO4↓+2H2O
171 9 8
x 100g×9.8%
$\frac{171}{x}=\frac{98}{100g×9.8%}$
解得x=17.1g
答案:
(1)①形成酸雨(或造成空气污染);②A;
(2)化工产品中残留Ba(OH)2的质量为17.1g.
点评 熟悉浓硫酸除具有酸的通性外,还有强氧化性、吸水性、脱水性,吸水性和脱水性的区别:吸水性吸的是游离态的水,脱水性脱的是氢氧原子按2:1形成的水.掌握利用化学方程式进行计算的方法步骤.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 能表示一个分子的是①④⑥ | |
| B. | ②⑤的质子数相同,化学性质也相同 | |
| C. | 表示物质组成的化学式是③④⑥ | |
| D. | ④中数字“5”表示是五氧化二磷中有5个氧原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答:
儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu、Mg | B. | Fe、Cu | C. | Cu | D. | Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
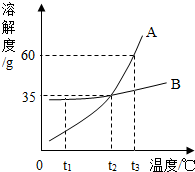 如图是A、B两种物质的溶解度曲线,下列说法中正确的是( )
如图是A、B两种物质的溶解度曲线,下列说法中正确的是( )| A. | A物质的溶解度为60g | |
| B. | t2℃时,两种物质的溶液溶质的质量分数相等 | |
| C. | t3℃时,等质量的两种物质的饱和溶液同时降温到t2℃时,析出晶体的质量关系是A>B | |
| D. | 升高温度可使不饱和的A溶液变为饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
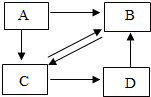
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com