
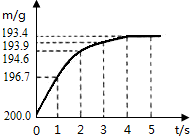
盛有12.60g碳酸氢钠固体的烧杯中,加入100.5g硫酸溶液恰好反应.反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始质量为200.0g.反应的化学方程式为:2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑.回答下列问题:

(1)当碳酸氢钠与硫酸溶液恰好完全反应时,所需的时间约为________.
(2)当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为________.
(3)反应后,所得硫酸钠溶液的溶质质量分数为多少?]
科目:初中化学 来源: 题型:解答题
 (相对分子质量:NaHCO3一84 H2SO4-98 Na2SO4-142 H2O一18 CO2一44)
(相对分子质量:NaHCO3一84 H2SO4-98 Na2SO4-142 H2O一18 CO2一44)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com