
| A、该反应不能作为判定Cu和Fe的金属活动性顺序的依据 |
| B、一定量的Cu与FeCl3溶液反应后的溶液中一定含有FeCl2和CuCl2,可能含有FeCl3 |
| C、金属Zn与FeCl3溶液的反应可类比推知,若反应后固体有剩余,则固体中一定含Fe,可能含Zn |
| D、一定量的Zn与FeCl3溶液反应后的溶液中一定含有FeCl2和ZnCl2,可能含有FeCl3 |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、29:8:13 |
| B、22:1:14 |
| C、13:8:29 |
| D、26:16:57 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
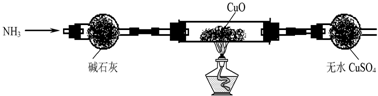
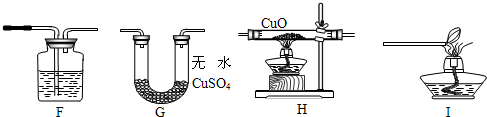
| H2SO4(浓) |
| △ |
| NaOH溶液 |
| O2 |
| △ |
| H2SO4(稀) |
| NaOH溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 |
| |
|
|
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图所示有一瓶刚收满的无色无毒气体.我对该瓶气体作出猜想,并想方设法验证它是何种气体?
如图所示有一瓶刚收满的无色无毒气体.我对该瓶气体作出猜想,并想方设法验证它是何种气体?| 验证方法 | 实验现象 | 结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com