(2013?河南模拟)(1)有如下反应:4FeS2+11O2=2R+8SO2,可以推断出物质R的化学式是:
(2)空气中含量最多的元素和地壳中含量最多的金属元素、非金属元素组成的化合物的化学式是:
(3)氮的某种氧化物中氮、氧元素质量之比为7:4;则此氧化物化学式是:.
【答案】
分析:(1)根据质量守恒定律的元素守恒,可推断反应前后的元素种类不变、原子个数不变,则可推测物质R的化学式;
(2)由题意“空气中含量最多的元素和地壳中含量最多的金属元素、非金属元素”,可推测其化合物的化学式;
(3)由题意“氮的某种氧化物中氮、氧元素质量之比为7:4”,可设其化学式,而推测其化学式的书写.
解答:解:(1)根据质量守恒定律的元素守恒,可推断反应前后的元素种类不变、原子个数不变,则:反应前4个铁原子、8个硫原子、22个氧原子;反应后已知二氧化硫中由8个硫原子、16个氧原子,则2R中含有4个铁原子、6个氧原子,故化学式为Fe
2O
3;
(2)由题意“空气中含量最多的元素和地壳中含量最多的金属元素、非金属元素”,则可知其组成元素为氮元素、铝元素、氧元素,故其化学式为Al(NO
3)
3;
(3)由题意“氮的某种氧化物中氮、氧元素质量之比为7:4”,可设氮的氧化物的化学式为NxOy,
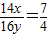
,解得
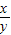
=

,故化学式为N
2O.
故答为:(1)Fe
2O
3;(2)Al(NO
3)
3;(3)N
2O
点评:根据化学方程式判断化学式,解题的根据是质量守恒定律,即反应前后原子的种类和数目不变;熟记地壳中前四位的元素含量排列;周围有关化学式的计算和推断方法.

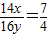 ,解得
,解得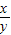 =
= ,故化学式为N2O.
,故化学式为N2O.
