
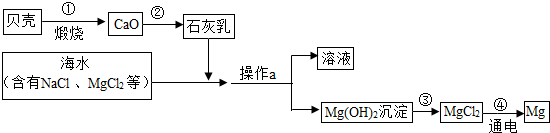
分析 高温条件下,碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙;
氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,氢氧化镁和稀盐酸反应生成氯化镁和水.
解答 解:(1)石灰乳在实际生活中有很多用途,例如可以用作建筑材料、制取波尔多液等.
故填:用作建筑材料.
(2)通过操作a后所得溶液中的溶质肯定含有氯化钠和反应生成的氯化钙.
故填:氯化钠、氯化钙.
(3)第③步中,氢氧化镁和稀盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O.
故填:Mg(OH)2+2HCl═MgCl2+2H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 化学兴趣小组的同学用如图所示装置进行中和反应实验,请你参与下列探究:
化学兴趣小组的同学用如图所示装置进行中和反应实验,请你参与下列探究:| 实验 | 实 验 方 法 | 实 验 现 象 | 实 验 结 论 |
| 甲 | 恰好中和 | ||
| 乙 | 第二种可能性 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.除杂的方法 | B.化学物质中的“三” |
| 粗盐提纯--溶解、过滤、蒸发 木炭粉中混有铁粉--用磁铁吸引 CO2中混有CO--通过灼热的氧化铜 | 三大化石燃料--煤、石油、天然气 三种碳素钢--高碳钢、中碳钢、低碳钢 三种黑色氧化物--氧化铜、二氧化锰、四氧化三铁 |
| C.实验安全注意事项 | D.化学物质与俗名 |
| 制取气体--先检查装置的气密性 点燃可燃性气体--先检验气体的纯度 进入久未开启的菜窖--先用“灯火试验” | 固体二氧化碳--干冰 氧化钙--生石灰 氢氧化钠--纯碱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com